题目内容
14.常温下,某同学设计实验验证H2SO3的酸性强于碳酸,下列实验方案能达到目的是( )| 选项 | 实验方案 | 实验结果 |
| A | 将SO2气体依次通过NaHCO3溶液、溴水、品红溶液、澄清石灰水 | 品红无变化,澄清石灰水变浑浊 |
| B | 将过量二氧化硫气体通入碳酸氢钠溶液中,逸出的气体通入澄清石灰水 | 澄清石灰水变浑浊 |
| C | 取相同体积、相同物质的量浓度的NaHSO3与Na2CO3溶液,分别加入等体积、等浓度的少量盐酸 | 前者产生气体体积大于后者的 |
| D | 分别配置SO2和CO2的饱和溶液,立即测定两种饱和液的pH | 前者的pH小于后者的 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.SO2和NaHCO3溶液反应生成CO2、SO2和溴水发生氧化还原反应生成H2SO4、SO2能使品红溶液褪色,当品红无变化时说明气体中不含SO2,CO2能使澄清石灰水变浑浊;
B.SO2、CO2都能使澄清石灰水变浑浊;
C.Na2CO3、NaHSO3分别和稀盐酸反应方程式为Na2CO3+2HCl=2NaCl+H2O+CO2↑、NaHSO3+HCl=NaCl+SO2↑+H2O,相同体积相同物质的量的浓度的碳酸钠和亚硫酸氢钠分别和等物质的量的盐酸反应,碳酸钠有剩余,根据原子守恒判断生成气体体积;
D.亚硫酸的酸性大于碳酸,且二氧化硫溶解度大于二氧化碳,二氧化硫、二氧化碳饱和溶液中c(H+)前者大于后者.
解答 解:A.SO2和NaHCO3溶液反应生成CO2、SO2和溴水发生氧化还原反应生成H2SO4、SO2能使品红溶液褪色,当品红无变化时说明气体中不含SO2,但CO2能使澄清石灰水变浑浊,所以可以得到实验结果品红无变化,澄清石灰水变浑浊,故A正确;
B.SO2、CO2都能使澄清石灰水变浑浊,逸出的气体能使澄清石灰水变浑浊不能是否含有二氧化碳,从而不能说明亚硫酸酸性大于碳酸,所以不能实现实验目的,故B错误;
C.Na2CO3、NaHSO3分别和稀盐酸反应方程式为Na2CO3+2HCl=2NaCl+H2O+CO2↑、NaHSO3+HCl=NaCl+SO2↑+H2O,相同体积相同物质的量的浓度的碳酸钠和亚硫酸氢钠分别和等物质的量的盐酸反应,碳酸钠有剩余,所以NaHSO3产生的气体大于Na2CO3,说明盐酸酸性大于亚硫酸、碳酸,但不能说明亚硫酸酸性大于碳酸,故C错误;
D.亚硫酸的酸性大于碳酸,且SO2溶解度大于CO2,SO2、CO2饱和溶液中c(H+)前者大于后者,则pH前者小于后者,故D正确;
故选AD.
点评 本题考查化学实验方案评价,为高频考点,明确实验原理及物质性质、物质性质差异性是解本题关键,注意:二氧化碳、二氧化硫都能使澄清石灰水变浑浊,不能用澄清石灰水鉴别二者,但可以用品红溶液鉴别二者,题目难度不大,易错选项是B.

| A. | 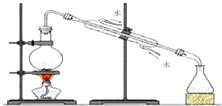 制取少量纯净的水 | B. |  除去Cl2中HCl杂质 | ||
| C. |  烧瓶内形成蓝色喷泉 | D. | 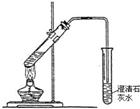 探究NaHCO3的热稳定性 |
| A. | 常温常压下,7.8gNa2S固体和7.8gNa2O2固体中含有的阴离子数目均为0.1NA | |
| B. | 在标准状况下,22.4LCl2和HCl的混合气体中含有的分子总数为2×6.02×1023 | |
| C. | 含1molFeCl3的饱和溶液滴入沸水中得到胶体数目为NA | |
| D. | 标准状况下,Na2O2与足量的CO2反应生成2.24LO2,转移电子数为0.4NA |
| A. | 元素丙的单质可用于冶炼金属 | |
| B. | 甲的氢化物比丁的氢化物热稳定性强 | |
| C. | 简单离子半径:乙>丁>丙 | |
| D. | 甲与乙的氧化物均有强氧化性 |
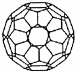
| A. | C60就是金刚石 | B. | C60属于有机化合物 | ||
| C. | C60的摩尔质量是720g/mol | D. | 1mol C60完全燃烧生成22.4L CO2 |
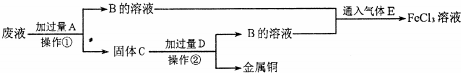
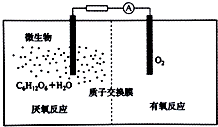 氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.
氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.