题目内容
11.下列各组混合物中,能用分液漏斗进行分离的是( )| A. | 酒精与水 | B. | 汽油与植物油 | C. | 溴与四氯化碳 | D. | 水与四氯化碳 |
分析 根据分液漏斗可以将互不相溶的两层液体分开,则分析选项中物质的溶解性即可.
解答 解:A.酒精和水能互溶,所以不能用分液漏斗分离,故A错误;
B.汽油与植物油能互溶,所以不能用分液漏斗分离,故B错误;
C.溴与四氯化碳能互溶,所以不能用分液漏斗分离,故C错误;
D.水和四氯化碳不溶,所以能用分液漏斗分离,故D正确.
故选D.
点评 本题考查物质的分离,题目难度不大,本题注意把握常见混合物的分离原理、方法以及操作的注意事项等.

练习册系列答案
相关题目
1.下列表示对应化学反应的离子方程式正确的是( )
| A. | NaHS溶液中通入Cl2:S2-+Cl2═S↓+2Cl- | |
| B. | NaN02溶液中滴加酸性KMnO4溶液:5NO2-+2MnO4-+3H2O═5NO3-+2Mn2++6OH- | |
| C. | NH4HSO4溶液中滴加少量的Ba(OH)2溶液:Ba2++2OH-+NH4++H++SO42-═BaSO4↓+NH3•H2O+H2O | |
| D. | 硫酸亚铁酸性溶液中加入过氧化氢:2Fe2++H2O2+2H+═2Fe3++2H2O |
2.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,7.8gNa2S固体和7.8gNa2O2固体中含有的阴离子数目均为0.1NA | |
| B. | 在标准状况下,22.4LCl2和HCl的混合气体中含有的分子总数为2×6.02×1023 | |
| C. | 含1molFeCl3的饱和溶液滴入沸水中得到胶体数目为NA | |
| D. | 标准状况下,Na2O2与足量的CO2反应生成2.24LO2,转移电子数为0.4NA |
19.C60自被发现以来,已逐步应用到超导、材料等各个领域.下列有关说法正确的是( )

| A. | C60就是金刚石 | B. | C60属于有机化合物 | ||
| C. | C60的摩尔质量是720g/mol | D. | 1mol C60完全燃烧生成22.4L CO2 |
16.下列物质中,属于酸性氧化物但不溶于水的是( )
| A. | 二氧化硫 | B. | 二氧化氮 | C. | 二氧化硅 | D. | 七氧化二氯 |
20.人们对未发现的第114号元素很感兴趣,预测它有良好的力学、光学、电学性质,它被命名为“类铅”.以下对“类铅”的叙述正确的是( )
| A. | 最外层有6个电子 | B. | 位于元素周期表的第七周期 | ||
| C. | 主要化合价为-4价、+4价 | D. | “类铅”不能和盐酸反应放出氢气 |
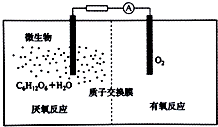 氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.
氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.