题目内容
8.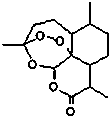 东晋医药学家葛洪的《肘后备急方•治寒热诸疟方》记载有“青蒿一握,以水二升渍,绞取汁,尽服之”的说法,说明不能加热青蒿,因高温可能使活性成分受损.中国药学家屠呦呦用沸点只有35℃的乙醚作为溶剂来提取青蒿素,创制出新型抗疟药青蒿素和双氢青蒿素,为此获得2015年诺贝尔生理学或医学奖.已知青蒿素的结构如图所示,下列有关青蒿素的说法,不正确的是( )
东晋医药学家葛洪的《肘后备急方•治寒热诸疟方》记载有“青蒿一握,以水二升渍,绞取汁,尽服之”的说法,说明不能加热青蒿,因高温可能使活性成分受损.中国药学家屠呦呦用沸点只有35℃的乙醚作为溶剂来提取青蒿素,创制出新型抗疟药青蒿素和双氢青蒿素,为此获得2015年诺贝尔生理学或医学奖.已知青蒿素的结构如图所示,下列有关青蒿素的说法,不正确的是( )| A. | 分子式为C15H22O5 | |
| B. | 能够发生水解反应 | |
| C. | 用沸点只有35℃的乙醚作为溶剂来提取青蒿素的方法化学上叫萃取 | |
| D. | 青蒿素能够治疗疟疾可能与结构中存在过氧键或酯基等基团有关 |
分析 A.根据结构简式确定分子式;
B.该分子中含有醚键、过氧键和酯基,酯基能发生水解反应;
C.用乙醚为溶剂在低温下从黄花蒿中提取青蒿素是利用了萃取;
D.过氧键具有强氧化性.
解答 解:A.根据结构简式确定分子式为C15H22O5,故A正确;
B.该分子中含有醚键、过氧键和酯基,酯基能发生水解反应,所以该物质能发生水解反应,故B正确;
C.用乙醚为溶剂在低温下从黄花蒿中提取青蒿素是利用其在有机物的溶解性较大,所以是利用了萃取原理,故C正确;
D.过氧键具有强氧化性,能使蛋白质变性而治疗疟疾,与酯基无关,故D错误;
故选D.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查酯、过氧键等官能团,题目难度不大.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
18.下列说法正确的是( )
| A. | SO2和CO都是酸性氧化物,都能与水反应 | |
| B. | Na2O和Na2O2组成元素相同,与CO2反应产物也完全相同 | |
| C. | Al2O3和Na2O按物质的量比1:1投入水中可得到澄清溶液 | |
| D. | 金属铝排在金属活动性顺序表中氢元素的前面,铝与强酸反应一定放出氢气 |
19.C60自被发现以来,已逐步应用到超导、材料等各个领域.下列有关说法正确的是( )

| A. | C60就是金刚石 | B. | C60属于有机化合物 | ||
| C. | C60的摩尔质量是720g/mol | D. | 1mol C60完全燃烧生成22.4L CO2 |
16.下列物质中,属于酸性氧化物但不溶于水的是( )
| A. | 二氧化硫 | B. | 二氧化氮 | C. | 二氧化硅 | D. | 七氧化二氯 |
13.豆类中的香豆雌酚是一种植物雌性激素,其结构式如图所示,下列有关说法正确的是( )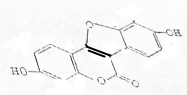

| A. | 该物质的分子式为C15H10O5 | |
| B. | 该物质中所有原子一定在同一平面内 | |
| C. | 1mol该物质最多可与5molBr2发生反应 | |
| D. | 1mol该物质最多可与3molNaOH发生反应 |
20.人们对未发现的第114号元素很感兴趣,预测它有良好的力学、光学、电学性质,它被命名为“类铅”.以下对“类铅”的叙述正确的是( )
| A. | 最外层有6个电子 | B. | 位于元素周期表的第七周期 | ||
| C. | 主要化合价为-4价、+4价 | D. | “类铅”不能和盐酸反应放出氢气 |
9. I.下表是A、B、C、D、E五种短周期元素的某些性质:
I.下表是A、B、C、D、E五种短周期元素的某些性质:
(1)E原子的外围电子排布式为2s22p5.
(2)与AD2互为等电子体的分子化学式为N2O(写出一种).
(3)BD2分子中B原子的杂化方式为sp2杂化,分子的立体构型为V形.
Ⅱ.下表是部分金属元素的电离能.
(4)已知X、Y、Z的价层电子构型为ns1,则三种金属的氯化物( RCl)的熔点由低到高的顺序为ZCl<YCl<XCl.
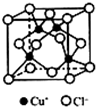
(5)氯化亚铜常用作有机合成催化剂,并用于颜料,防腐等工业.氯化亚铜的晶体结构如图所示.与同一个Cl-相连的Cu+有4个.若晶胞的边长为a cm,则该品体的密度为$\frac{398}{{N}_{A}×{a}^{3}}$g•cm-3.(设NA为阿伏加德罗常数的值)
 I.下表是A、B、C、D、E五种短周期元素的某些性质:
I.下表是A、B、C、D、E五种短周期元素的某些性质:| A | B | C | D | E | |
| 化合价 | -4 | -2 | -1 | -2 | -1 |
| 电负性 | 2.5 | 2.5 | 3.0 | 3.5 | 4.0 |
(2)与AD2互为等电子体的分子化学式为N2O(写出一种).
(3)BD2分子中B原子的杂化方式为sp2杂化,分子的立体构型为V形.
Ⅱ.下表是部分金属元素的电离能.
| X | Y | Z | |
| 第一电离能/(kJ/mol) | 520.2 | 495.8 | 418.8 |
(5)氯化亚铜常用作有机合成催化剂,并用于颜料,防腐等工业.氯化亚铜的晶体结构如图所示.与同一个Cl-相连的Cu+有4个.若晶胞的边长为a cm,则该品体的密度为$\frac{398}{{N}_{A}×{a}^{3}}$g•cm-3.(设NA为阿伏加德罗常数的值)
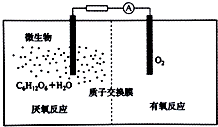 氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.
氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.