题目内容
7.下列叙述一定正确的是( )| A. | 两份质量相同的镁分别与足量氮气、二氧化碳反应,增重的质量相同 | |
| B. | 两份质量相同的硫分别与足量氢氧化钠和钠反应,两者转移的电子数相同 | |
| C. | 相同物质的量CO2、H2O分别与足量Na2O2反应,生成气体的体积相同 | |
| D. | 氢气分别通过灼热的CuO和Fe2O3粉末,当转移电子数相同时,固体减轻的质量相同 |
分析 A、镁和氮气生成氮化镁、镁与二氧化碳反应生成氧化镁,由此分析;
B、硫与氢氧化钠反应是自身的氧化还原反应,而与单质钠反应是仅作氧化剂;
C、由发生反应:2Na2O2+2CO2=Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑分析;
D、氢气分别通过灼热的CuO和Fe2O3粉末,氢气夺取氧化物中的氧,转化为水,当转移电子数相同时说明参加反应的氢气的物质的量相等,夺氧的质量相同.
解答 解:A、镁和氮气生成氮化镁、镁与二氧化碳反应生成氧化镁,设1mol的镁增重为$\frac{2}{3}×14$=9.3g,而1mol的镁与0.5mol的二氧化碳反应生成氧化镁和单碳,增重为:0.5mol×44g/mol=22g,所以增重不等,故A错误;
B、硫与氢氧化钠反应是自身的氧化还原反应,而与单质钠反应是仅作氧化剂,所以两份质量相同的硫分别与足量氢氧化钠和钠反应,两者转移的电子数不相同,故B错误;
C、由发生反应:2Na2O2+2CO2=Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑,所以相同物质的量CO2、H2O分别与足量Na2O2反应,生成气体的物质的量相同,在相同条件下体积相同,故C错误;
D、氢气分别通过灼热的CuO和Fe2O3粉末,氢气夺取氧化物中的氧,转化为水,当转移电子数相同时说明参加反应的氢气的物质的量相等,夺氧的质量相同,所以固体减轻的质量相同,故D正确;
故选D.
点评 本题考查元素及化合物的综合应用,为高频考点,把握发生的反应及氧化还原反应的分析为解答的关键,侧重分析、计算及应用能力的考查,题目难度不大.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
17.同位素的发现能揭示物质微观结构与性质之间的关系.下列说法正确的是( )
| A. | O2和O3互为同位素 | B. | 1个15O2中含有18个中子 | ||
| C. | 18O2与16O2的性质完全相同 | D. | 16O和18O的核外电子数相同 |
18.下列说法正确的是( )
| A. | SO2和CO都是酸性氧化物,都能与水反应 | |
| B. | Na2O和Na2O2组成元素相同,与CO2反应产物也完全相同 | |
| C. | Al2O3和Na2O按物质的量比1:1投入水中可得到澄清溶液 | |
| D. | 金属铝排在金属活动性顺序表中氢元素的前面,铝与强酸反应一定放出氢气 |
2.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,7.8gNa2S固体和7.8gNa2O2固体中含有的阴离子数目均为0.1NA | |
| B. | 在标准状况下,22.4LCl2和HCl的混合气体中含有的分子总数为2×6.02×1023 | |
| C. | 含1molFeCl3的饱和溶液滴入沸水中得到胶体数目为NA | |
| D. | 标准状况下,Na2O2与足量的CO2反应生成2.24LO2,转移电子数为0.4NA |
12.有机物M是合成二氢荆芥内酯的重要原料,结构简式为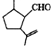 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A. | M的分子式为C10H14O | |
| B. | M能发生氧化反应,不能发生还原反应 | |
| C. | M与FeCl3溶液反应生成紫色有机化合物 | |
| D. | 检验M中官能团是先加入新制氢氧化铜,微热,酸化后再加溴水 |
19.C60自被发现以来,已逐步应用到超导、材料等各个领域.下列有关说法正确的是( )

| A. | C60就是金刚石 | B. | C60属于有机化合物 | ||
| C. | C60的摩尔质量是720g/mol | D. | 1mol C60完全燃烧生成22.4L CO2 |
16.下列物质中,属于酸性氧化物但不溶于水的是( )
| A. | 二氧化硫 | B. | 二氧化氮 | C. | 二氧化硅 | D. | 七氧化二氯 |
