题目内容
17.某溶液中只含有Na+、Fe3+、Cl-三种离子,其中Na+的物质的量为0.01mol,Fe3+的物质的量为0.04mol,在此溶液中加入0.03mol氢氧化钠,则最后溶液中的Na+与Cl-的数目之比为( )| A. | 4:13 | B. | 1:13 | C. | 1:3 | D. | 13:4 |
分析 Na+的物质的量为0.01mol,Fe3+的物质的量为0.04mol,由电荷守恒可知,Cl-的物质的量为0.01+0.04×3=0.13mol,在此溶液中加入0.03mol氢氧化钠,则最后溶液中的Na+为0.04mol,而Cl-不变,以此来解答.
解答 解:Na+的物质的量为0.01mol,Fe3+的物质的量为0.04mol,由电荷守恒可知,Cl-的物质的量为0.01+0.04×3=0.13mol,在此溶液中加入0.03mol氢氧化钠,溶液中的Na+为0.04mol,而Cl-不变,则最后溶液中的Na+与Cl-的数目之比为0.04mol:0.13mol=4:13,
故选A.
点评 本题考查物质的量的计算,为高频考点,把握电荷守恒及离子的变化为解答的关键,侧重分析与计算能力的考查,注意电荷守恒的应用,题目难度不大.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
7.如图所示的装置中,金属片紧靠贴着滤纸,下列判断错误的是( )
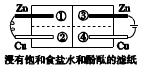

| A. | 两处的锌片均发生氧化反应 | |
| B. | 左侧铜片上的电极反应为2H2O+O2+4e-═4OH- | |
| C. | 阳离子移动方向分别由②→①、③→④ | |
| D. | 最先观察到红色的区域是④ |
8.下列离子方程式正确的是( )
| A. | SO2与酸性KMnO4溶液的反应:5SO2+2MnO4-+2H2O═5SO42-+2Mn2++4H+ | |
| B. | 稀硫酸和氢氧化钡溶液反应:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| C. | 硝酸银溶液中滴加过量氨水:Ag++NH3•H2O═AgOH↓+NH4+ | |
| D. | 石灰水与过量碳酸氢钠溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
5.有物质的量浓度均为0.1mol•L-1 的①Na2CO3溶液 ②CH3COONa溶液 ③NaOH溶液各25mL,下列说法正确的是( )
| A. | 3种溶液pH的大小顺序是 ③>②>① | |
| B. | 若将3种溶液稀释相同倍数,pH变化最大的是① | |
| C. | 若分别加入25mL 0.1mol•L-1盐酸后,pH最小的是② | |
| D. | 若升高温度,则③的pH不变 |
12.在强碱性溶液中,下列各组离子能在同一溶液里大量共存的是( )
| A. | Na+、Al3+、Cl- | B. | K+、H+、SO42- | C. | Na+、HCO3-、NO3- | D. | K+、Na+、AlO2- |
2.下列叙述错误的是( )
| A. | 用丁达尔现象区分溶液与胶体 | |
| B. | 用蒸馏的方法除去自来水中含有的Cl- | |
| C. | 用萃取的方法从某些植物中提取香料或中药成份 | |
| D. | 金属钠长期暴露在空气中的最终产物是NaHCO3 |
4.标准状况下VL氨气溶解在1L水中,所得溶液的密度为ρ g/ml,质量分数为ω,物质浓度为c mol/L,则下列关系中正确的是( )
| A. | c=$\frac{Vρ}{17V+22400}$ | B. | ω=$\frac{17c}{100ρ}$ | ||
| C. | ω=$\frac{17V}{17V+22400}$ | D. | ρ=$\frac{17V+22400}{22.4+22.4V}$ |
1.下列有关金属及其化合物的说法正确的是( )
| A. | Mg和Al都可以用电解法冶炼得到 | |
| B. | Na2O2、Na2O组成元素相同,与CO2反应产物也相同 | |
| C. | 用过量的KSCN溶液除去FeCl2溶液中的少量FeCl3 | |
| D. | Na和Fe在一定条件下与水反应都生成H2和对应的碱 |
2.同温同压下,三个等体积的干燥圆底烧瓶中分别充满:①混有少量空气的HCl;②NO2;③体积比为4:1的NO2和O2,进行喷泉实验.经充分反应后烧瓶内溶质的物质的量浓度之比为( )
| A. | 1:1:1 | B. | 4:4:5 | C. | 5:5:4 | D. | 无法确定 |