题目内容
2.下列叙述错误的是( )| A. | 用丁达尔现象区分溶液与胶体 | |
| B. | 用蒸馏的方法除去自来水中含有的Cl- | |
| C. | 用萃取的方法从某些植物中提取香料或中药成份 | |
| D. | 金属钠长期暴露在空气中的最终产物是NaHCO3 |
分析 A.丁达尔现象为胶体特有的性质;
B.自来水中水的沸点低;
C.香料或中药成份易溶于有机溶剂,不易溶于水;
D.金属钠长期暴露在空气中,氧化生成氧化钠,再与水反应生成NaOH,吸收空气中的二氧化碳反应生成碳酸钠,形成晶体风化最终为Na2CO3.
解答 解:A.丁达尔现象为胶体特有的性质,则丁达尔现象可区分溶液与胶体,故A正确;
B.自来水中水的沸点低,则蒸馏的方法可除去自来水中含有的Cl-,故B正确;
C.香料或中药成份易溶于有机溶剂,不易溶于水,则萃取的方法可从某些植物中提取香料或中药成份,故C正确;
D.金属钠长期暴露在空气中的最终产物是Na2CO3,故D错误;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、物质的鉴别、混合物分离提纯为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识与实验的结合,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.认真观察下列装置,下列说法错误的是( )
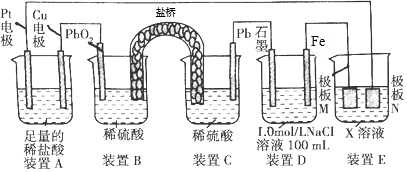

| A. | 装置B中PbO2上发生的电极反应方程式为:PbO2+4H++SO42-+2e-═PbSO4+2H2O | |
| B. | 装置A中总反应的离子方程式为:Cu+2H+$\frac{\underline{\;通电\;}}{\;}$Cu2++H2↑ | |
| C. | 若装置E的目的是在Cu材料上镀银,则极板N的材料为Cu | |
| D. | 若在装置D中生成0.2molFe(OH)3,则消耗水的物质的量共为0.5mol |
13.一定条件下,对于可逆反应X(g)+3Y(g)?2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1mol/L、0.3mol/L、0.08mol/L,则下列判断正确的是( )
| A. | X、Y的转化率相等 | |
| B. | 在恒温恒压条件下,达到平衡后充入Y气体,则平衡正向移动 | |
| C. | 平衡时,Y和Z的生成速率之比为2:3 | |
| D. | c1的取值范围为0.04 mol/L<c1<0.14 mol/L |
10.下列电离方程式正确的是( )
| A. | CH3COOH=H++CH3COO- | B. | HClO?H++ClO- | ||
| C. | H2SO4 $\frac{\underline{\;通电\;}}{\;}$=2H++SO42- | D. | Ca(OH)2?Ca2++(OH-)2 |
17.某溶液中只含有Na+、Fe3+、Cl-三种离子,其中Na+的物质的量为0.01mol,Fe3+的物质的量为0.04mol,在此溶液中加入0.03mol氢氧化钠,则最后溶液中的Na+与Cl-的数目之比为( )
| A. | 4:13 | B. | 1:13 | C. | 1:3 | D. | 13:4 |
2.氙气和氟气在一定条件下可反应达到平衡:Xe(g)+2F2(g)?XeF4(g)△H=-218kJ/mol.下列变化既能加快反应速率又能使平衡向正反应方向移动的是( )
| A. | 升高温度 | B. | 减压 | C. | 加压 | D. | 适当降温 |
9.电离平衡常数是衡量弱电解质电离程度的量.已知如下表数据(25℃):
(1)25℃时,等浓度的三种溶液(A.NaCN溶液、B.Na2CO3溶液、C.CH3COONa溶液)的pH由大到小的顺序为b>a>c.(填写序号)
(2)25℃时,向NaCN溶液中通入少量CO2,所发生反应的化学方程式为NaCN+CO2+H2O=NaHCO3+HCN.
(3)现有浓度为0.02mol/L的HCN与0.01mol/L NaOH等体积混合后,测得c(Na+)>c(CN-),下列关系正确的是BD.
A.c(H+)>c(OH-)
B.c(H+)<c(OH-)
C.c(H+)+c(HCN)=c(OH-)
D.c(HCN)+c(CN-)=0.01mol/L
(4)浓的Al2(SO4)3溶液和浓的小苏打(NaHCO3)溶液混合可用于灭火,请用离子反应方程式表示灭火的原理Al3++3HCO3-=Al(OH)3↓+3CO2↑.
(5)已知NaHC2O4水溶液显酸性,请写出该溶液中各离子浓度的大小c(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-).
| 化学式 | 电离平衡常数 |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.4×10-7,K2=4.7×10-11 |
(2)25℃时,向NaCN溶液中通入少量CO2,所发生反应的化学方程式为NaCN+CO2+H2O=NaHCO3+HCN.
(3)现有浓度为0.02mol/L的HCN与0.01mol/L NaOH等体积混合后,测得c(Na+)>c(CN-),下列关系正确的是BD.
A.c(H+)>c(OH-)
B.c(H+)<c(OH-)
C.c(H+)+c(HCN)=c(OH-)
D.c(HCN)+c(CN-)=0.01mol/L
(4)浓的Al2(SO4)3溶液和浓的小苏打(NaHCO3)溶液混合可用于灭火,请用离子反应方程式表示灭火的原理Al3++3HCO3-=Al(OH)3↓+3CO2↑.
(5)已知NaHC2O4水溶液显酸性,请写出该溶液中各离子浓度的大小c(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-).
6.下列叙述不正确的是( )
| A. | 铁制品表面镀锌可以增强其抗腐蚀性 | |
| B. | 在海轮外壳上连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 | |
| C. | 有些合金比纯净的金属耐腐蚀 | |
| D. | 利用外加电流的阴极保护法,可以将水下的钢闸门与电源正极相连 |