题目内容
7.如图所示的装置中,金属片紧靠贴着滤纸,下列判断错误的是( )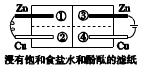
| A. | 两处的锌片均发生氧化反应 | |
| B. | 左侧铜片上的电极反应为2H2O+O2+4e-═4OH- | |
| C. | 阳离子移动方向分别由②→①、③→④ | |
| D. | 最先观察到红色的区域是④ |
分析 A、左边是构原电池,活泼的锌是负极;右边是电解池,锌是阳极,发生氧化反应;
B、左侧是发生吸氧腐蚀;
C、原电池中阳离子向正极移动,电解池中阳离子向阴极移动;
D、左边为原电池,右边为电解池,电解池中的反应速率快.
解答 A、左边是构原电池,活泼的锌是负极;右边是电解池,锌是阳极,发生氧化反应,所以两处的锌片均发生氧化反应,故A正确;
B、左侧是发生吸氧腐蚀,电极反应式为:2H2O+O2+4e-═4OH-,故B正确;
C、原电池中阳离子向正极移动,电解池中阳离子向阴极移动,所以阳离子移动方向分别由①→②、③→④,故C错误;
D、左边为原电池,右边为电解池,电解池中的反应速率快,所以最先观察到红色的区城是④,故D正确;
故选C.
点评 本题考查了原电池原理和电解池原理的应用,题目难度不大,注意把握电极的判断和电极方程式的书写.

练习册系列答案
 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
17.下列有关化学用语表示正确的是( )
| A. | 过氧化钠的电子式: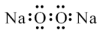 | B. | 次氯酸的结构式:H-Cl-O | ||
| C. | NH4Cl的电子式: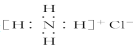 | D. | 硫原子的结构示意图: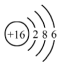 |
15.常温下,下列各组比值为1:2的是( )
| A. | 0.1mol•L-1与0.2mol•L-1醋酸溶液,c(H+)之比 | |
| B. | 0.1mol•L-1Na2HPO4溶液,c(HPO42-)与c(Na+)之比 | |
| C. | pH=10的Ba(OH)2溶液与氨水,溶质的物质的量浓度之比 | |
| D. | pH=3的硫酸与醋酸溶液,c(SO42-)与c(CH3COO-)之比 |
2.下列离子方程式中正确的是( )
| A. | 碳酸钠加入醋酸溶液中:CO32-+2H+═H2O+CO2↑ | |
| B. | NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-═CO32-+H2O | |
| C. | Ba(OH)2加入过量NaHCO3溶液中:Ba2++2OH-+2HCO3-═BaCO3↓+CO32-+2H2O | |
| D. | 铜粉投入FeCl3溶液中:Fe3++Cu═Fe2++Cu2+ |
12.认真观察下列装置,下列说法错误的是( )
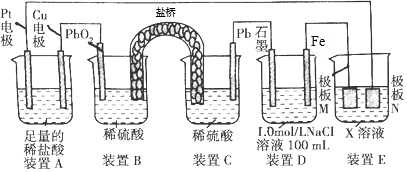

| A. | 装置B中PbO2上发生的电极反应方程式为:PbO2+4H++SO42-+2e-═PbSO4+2H2O | |
| B. | 装置A中总反应的离子方程式为:Cu+2H+$\frac{\underline{\;通电\;}}{\;}$Cu2++H2↑ | |
| C. | 若装置E的目的是在Cu材料上镀银,则极板N的材料为Cu | |
| D. | 若在装置D中生成0.2molFe(OH)3,则消耗水的物质的量共为0.5mol |
19.下列化学用语错误的是( )
| A. | 氯化氢分子的电子式: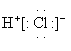 | B. | 乙烯的结构简式:CH2=CH2 | ||
| C. | 苯的分子式:C6H6 | D. | 氯的原子结构示意图: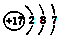 |
16.下列化学反应表达错误的是( )
| A. | CH2=CH2+HBr $\stackrel{催化剂}{→}$CH3CH2Br | |
| B. | CH3COOH+CH3CH2OH $?_{△}^{浓硫酸}$CH3COOC2H5 | |
| C. | 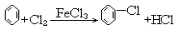 | |
| D. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O |