题目内容
将一定量xAl2(SO4)3?y(NH4)2SO4?24H2O晶体加入到过量NaOH溶液中,加热生成NH3 0.85g(假如生成的NH3全部逸出),再通入过量的CO2,过滤、洗涤、灼烧,得Al2O3固体2.55g.则x:y=(已知:Al2O3的相对分子质量为102;NH3的相对分子质量为17)( )
| A、1:2 | B、1:1 |
| C、1:4 | D、2:1 |
考点:复杂化学式的确定
专题:计算题
分析:根据质量守恒定律可知,晶体中的氮元素和氨气中的氮元素的质量相等,而晶体中的铝元素的质量和生成的氧化铝中的铝元素的质量相等,可以据此结合元素的质量比的计算方法列出等式,求出x、y的质量比即可.
解答:
解:根据质量守恒定律可知,晶体中的N元素和氨气中的N元素的质量相等,而晶体中的Al元素的质量和生成的氧化铝中的Al元素的质量相等,
则:(27×2)x:(14×2)y=(2.55g×
×100%):(0.85g×
×100%),
解得:x:y=1:1,
故选B.
则:(27×2)x:(14×2)y=(2.55g×
| 54 |
| 102 |
| 14 |
| 17 |
解得:x:y=1:1,
故选B.
点评:本题考查了复杂化学式的确定方法,题目难度不大,注意掌握质量守恒定律的含义及在化学计算中的应用方法,明确xAl2(SO4)3?y(NH4)2SO4?24H2O中铝元素、氮元素与氨气、氧化铝的关系为解答关键.

练习册系列答案
相关题目
下列基态原子的电子排布式中,其未成对电子数最多的是( )
| A、1s22s22p63s23p63d54s1 |
| B、1s22s22p63s23p3 |
| C、1s22s22p63s23p63d64s2 |
| D、1s22s22p63s23p63d74s2 |
某主族元素原子的第一、二、三、四各级电离能依次为:899KJ/mol、1757KJ/mol、14840KJ/mol、18025KJ/mol,试分析该元素所在的族序数为( )
| A、IA族 | B、ⅡA族 |
| C、ⅢA族 | D、IVA族 |
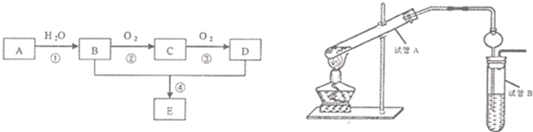
下列各选项最后的物质是要制取的物质,其中能够得到的是( )
A、CaCO3
| ||||||||
B、Cu
| ||||||||
C、KMnO4
| ||||||||
D、NH3
|
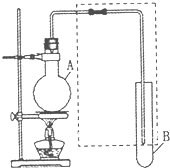 如图是用于简单有机化合物的制备、分离、性质比较等的常见简易装置.请
如图是用于简单有机化合物的制备、分离、性质比较等的常见简易装置.请