题目内容
 如图是用于简单有机化合物的制备、分离、性质比较等的常见简易装置.请
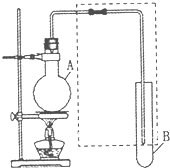
如图是用于简单有机化合物的制备、分离、性质比较等的常见简易装置.请根据该装置回答下列问题:
(1)若用乙醇与乙酸反应制取乙酸乙酯,则烧瓶A中加入的试剂在混合时的操作方法是
(2)若用该装置分离乙酸和1-丙醇,则在烧瓶A中除加入1-丙醇与乙酸外,还应先加入适量的试剂
(3)若用该装置(不用加热)证明酸性:醋酸>碳酸>苯酚,则在烧瓶A中加入
考点:乙酸乙酯的制取,物质的分离、提纯的基本方法选择与应用
专题:实验设计题
分析:(1)类比浓硫酸的稀释操作解答,先加入乙醇,然后加入浓硫酸,冷却后加入乙酸;乙酸与乙醇在浓硫酸作用下加热反应生成乙酸乙酯;用饱和碳酸钠溶液分离混合物;长导管起到导气和冷凝乙酸丙酯蒸汽的作用;
(2)先把酸转化为盐溶液,再蒸馏,馏分为丙醇,剩余的水溶液中加硫酸得到乙酸,再通过蒸馏分离;
(3)烧瓶A中加入苯酚钠和醋酸,反应生成二氧化碳气体,证明酸性醋酸>碳酸,生成的二氧化碳通入盛有苯酚钠溶液试管B中,溶液变浑浊,证明酸性碳酸>苯酚.
(2)先把酸转化为盐溶液,再蒸馏,馏分为丙醇,剩余的水溶液中加硫酸得到乙酸,再通过蒸馏分离;
(3)烧瓶A中加入苯酚钠和醋酸,反应生成二氧化碳气体,证明酸性醋酸>碳酸,生成的二氧化碳通入盛有苯酚钠溶液试管B中,溶液变浑浊,证明酸性碳酸>苯酚.
解答:
解:(1)为防止酸液飞溅,应将密度大的液体加入到密度小的液体中,乙酸易挥发,冷却后再加入乙酸;
酯化反应的本质为酸脱羟基,醇脱氢,乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应为可逆反应为:CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;
生成的乙酸乙酯蒸汽中含有乙醇和乙酸,要用饱和碳酸钠溶液分离混合物;长导管起到导气和冷凝乙酸丙酯蒸汽的作用;
故答案为:先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,冷却后再加乙酸;CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O;饱和碳酸钠溶液;冷凝;
CH3COOCH2CH3+H2O;饱和碳酸钠溶液;冷凝;
(2)在乙酸和1-丙醇的混合液中加入CaO,把乙酸转化为盐溶液,加热蒸馏,试管B中收集到的馏分为丙醇,烧瓶中剩余的为乙酸钙的水溶液,再加浓硫酸得到乙酸,通过蒸馏分离得到乙酸,
故答案为:CaO;CH3CH2CH2OH;浓硫酸;CH3COOH;
(3)在烧瓶A中加入苯酚钠和醋酸,有气泡产生,说明反应生成二氧化碳气体,证明酸性:醋酸>碳酸;将生成的二氧化碳通入盛有苯酚钠溶液试管B中,溶液变浑浊,证明酸性:碳酸>苯酚,
故答案为:碳酸钠和醋酸;苯酚钠溶液.
酯化反应的本质为酸脱羟基,醇脱氢,乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应为可逆反应为:CH3COOH+CH3CH2OH
 CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;生成的乙酸乙酯蒸汽中含有乙醇和乙酸,要用饱和碳酸钠溶液分离混合物;长导管起到导气和冷凝乙酸丙酯蒸汽的作用;
故答案为:先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,冷却后再加乙酸;CH3COOH+CH3CH2OH
 CH3COOCH2CH3+H2O;饱和碳酸钠溶液;冷凝;
CH3COOCH2CH3+H2O;饱和碳酸钠溶液;冷凝;(2)在乙酸和1-丙醇的混合液中加入CaO,把乙酸转化为盐溶液,加热蒸馏,试管B中收集到的馏分为丙醇,烧瓶中剩余的为乙酸钙的水溶液,再加浓硫酸得到乙酸,通过蒸馏分离得到乙酸,
故答案为:CaO;CH3CH2CH2OH;浓硫酸;CH3COOH;
(3)在烧瓶A中加入苯酚钠和醋酸,有气泡产生,说明反应生成二氧化碳气体,证明酸性:醋酸>碳酸;将生成的二氧化碳通入盛有苯酚钠溶液试管B中,溶液变浑浊,证明酸性:碳酸>苯酚,
故答案为:碳酸钠和醋酸;苯酚钠溶液.
点评:本题考查了有机物的制备、分离和提纯,题目难度中等,试题侧重于基本实验操作的考查,注意把握有关物质的性质,试题有利于提高学生灵活应用所学知识的能力.

练习册系列答案
相关题目
元素X原子的价电子排布为ns1,元素Y和Z的基态原子2p轨道上均有两个未成对电子,且原子序数为Y大于Z.则X、Y、Z三种元素组成的化合物的分子式不可能是( )
| A、X2ZY3 |
| B、X4Y2Z2 |
| C、X3YZ |
| D、X4ZY |
今有一混合物的水溶液,只可能含有以下离子中的若干种:Na+、NH4+、Ba2+、Cl-、CO32-、SO42-,现取两份200mL溶液进行如下实验:
①第一份加足量NaOH溶液,加热,收集到气体1.792L(已换算成标准状况,且设气体全部逸出);
②第二份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g.
据上述实验,以下推测正确是( )
①第一份加足量NaOH溶液,加热,收集到气体1.792L(已换算成标准状况,且设气体全部逸出);
②第二份加足量BaCl2溶液后,得干燥沉淀12.54g,经足量盐酸洗涤、干燥后,沉淀质量为4.66g.
据上述实验,以下推测正确是( )
| A、一定不存在Ba2+,NH4+可能存在 |
| B、CO32- 一定存在 |
| C、Na+一定不存在 |
| D、一定不存在Cl- |
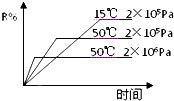 在密闭容器中进行下列反应:M(g)+N(g)?R(g)+2X(?),该反应中R的体积分数如图所示,下列情况正确的是( )
在密闭容器中进行下列反应:M(g)+N(g)?R(g)+2X(?),该反应中R的体积分数如图所示,下列情况正确的是( )| A、正反应为吸热反应,X为气体 |
| B、正反应为吸热反应,X为固体或液体 |
| C、正反应为放热反应,X为气体 |
| D、正反应为放热反应,X为固体或液体 |
自然界地表层铜的硫化物经氧化、淋滤作用后变成CuSO4溶液,向地下层渗透,遇到难溶的ZnS,慢慢转变为CuS.下列分析正确的是( )
| A、铜的硫化物具有氧化性 |
| B、CuS的溶解度大于ZnS的溶解度 |
| C、CuSO4与ZnS反应的离子方程式是Cu2++S2-=CuS↓ |
| D、以上过程涉及到了氧化还原反应和复分解反应 |