题目内容
下列基态原子的电子排布式中,其未成对电子数最多的是( )
| A、1s22s22p63s23p63d54s1 |
| B、1s22s22p63s23p3 |
| C、1s22s22p63s23p63d64s2 |
| D、1s22s22p63s23p63d74s2 |
考点:原子核外电子排布
专题:原子组成与结构专题
分析:根据各个原子中未成对电子个数判断,当原子中每个能级上电子处于半满时,该能级中未成对电子数最多,据此分析解答.
解答:
解:A.1s22s22p63s23p63d54s1中未成对电子数是6;
B.1s22s22p63s23p3中未成对电子数是3;
C.1s22s22p63s23p63d64s2中未成对电子数是4;
D.1s22s22p63s23p63d74s2中未成对电子数是3;
通过以上分析知,原子中未成对电子数最多的是A,
故选A.
B.1s22s22p63s23p3中未成对电子数是3;
C.1s22s22p63s23p63d64s2中未成对电子数是4;
D.1s22s22p63s23p63d74s2中未成对电子数是3;
通过以上分析知,原子中未成对电子数最多的是A,
故选A.
点评:本题考查了原子核外电子排布,知道原子轨道中电子处于半满时未成对电子数最多是解题的关键.

练习册系列答案
相关题目
元素X原子的价电子排布为ns1,元素Y和Z的基态原子2p轨道上均有两个未成对电子,且原子序数为Y大于Z.则X、Y、Z三种元素组成的化合物的分子式不可能是( )
| A、X2ZY3 |
| B、X4Y2Z2 |
| C、X3YZ |
| D、X4ZY |
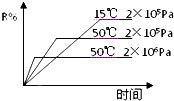 在密闭容器中进行下列反应:M(g)+N(g)?R(g)+2X(?),该反应中R的体积分数如图所示,下列情况正确的是( )
在密闭容器中进行下列反应:M(g)+N(g)?R(g)+2X(?),该反应中R的体积分数如图所示,下列情况正确的是( )| A、正反应为吸热反应,X为气体 |
| B、正反应为吸热反应,X为固体或液体 |
| C、正反应为放热反应,X为气体 |
| D、正反应为放热反应,X为固体或液体 |
自然界地表层铜的硫化物经氧化、淋滤作用后变成CuSO4溶液,向地下层渗透,遇到难溶的ZnS,慢慢转变为CuS.下列分析正确的是( )
| A、铜的硫化物具有氧化性 |
| B、CuS的溶解度大于ZnS的溶解度 |
| C、CuSO4与ZnS反应的离子方程式是Cu2++S2-=CuS↓ |
| D、以上过程涉及到了氧化还原反应和复分解反应 |
下列各组离子中电子层结构相同的是( )
| A、S2-、Cl-、K+ |
| B、Na+、Cl-、Mg2+ |
| C、Cl-、Mg2+、Al3+ |
| D、Li+、O2-、F- |
 如图所示,甲、乙之间的隔板K可以左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处.在一定条件下发生可逆反应:2A(g)+B(g)?2C(g),反应达到平衡后,恢复到反应发生前时的温度.下列有关说法不正确的是( )
如图所示,甲、乙之间的隔板K可以左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处.在一定条件下发生可逆反应:2A(g)+B(g)?2C(g),反应达到平衡后,恢复到反应发生前时的温度.下列有关说法不正确的是( )| A、根据隔板K滑动与否可判断左右两边的反应是否达到平衡 |
| B、达到平衡后,隔板K最终停留在左侧刻度0--2之间 |
| C、到达平衡时,甲容器中C的物质的量大于乙容器中C的物质的量 |
| D、若平衡时K停留在左侧1处,则活塞仍停留在右侧6处 |
X、Y为两种元素的原子,X的阴离子与Y的阳离子具有相同的电子层结构,由此可知( )
| A、X的原子半径大于Y的原子半径 |
| B、X的电负性小于Y的电负性 |
| C、X的阴离子半径大于Y的阳离子半径 |
| D、X的I1小于Y 的I1 |