题目内容
1.设NA代表阿伏加德罗常数,下列说法正确的是( )| A. | 2.4 g金属镁变成镁离子时失去的电子数目为0.1NA | |
| B. | 2 g氢气所含原子数目为NA | |
| C. | 1 mol MgCl2固体溶于水中,所得氯离子的数目为NA | |
| D. | 17 g氨气所含电子数目为10NA |
分析 A、求出镁的物质的量,然后根据镁变为+2价来分析;
B、氢气由氢原子构成;
C、1mol氯化镁中含2mol氯离子;
D、求出氨气的物质的量,然后根据氨气中含10个电子来分析.
解答 解:A、2.4g镁的物质的量为0.1mol,而镁变为+2价,故0.1mol镁失去0.2NA个电子,故A错误;
B、氢气由氢原子构成,故2g氢气中含有的氢原子的物质的量为2mol,个数为2NA个,故B错误;
C、1mol氯化镁中含2mol氯离子,故1mol氯化镁溶于水后溶液中的氯离子的个数为2NA个,故C错误;
D、17g氨气的物质的量为1mol,而氨气中含10个电子,故1mol氨气中含10NA个电子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
相关题目
12.如图所示实验操作不正确的是( )
| A. | 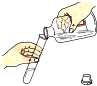 倾倒液体 | B. | 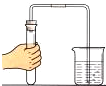 检查气密性 | C. | 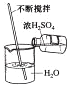 稀释浓硫酸 | D. | 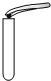 取用固体 |
9.下列事实能用勒夏特列原理解释的是( )
| A. | 在合成氨的工业生产中,使用较高温度有利于提高产量 | |
| B. | 在合成氨的工业生产中,加压有利于提高氨的产量 | |
| C. | 木炭粉碎后与O2反应,速率更快 | |
| D. | 由H2(g)、I2(g)、HI气体组成的平衡体系加压后颜色变深 |
16.0.5L 1molL-1FeCl3溶液与0.1L 1molL-1MgCl2溶液中Cl-的数目之比( )
| A. | 5:2 | B. | 3:1 | C. | 15:2 | D. | 1:3 |
6.以下几个热化学方程式,能表示固态碳和气态氢气燃烧时的燃烧热的热化学方程式是( )
| A. | C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=+110.5 kJ•mol-1 | |
| B. | C(s)+O2(g)═CO2(g)△H=-393.5 kJ•mol-1 | |
| C. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1 | |
| D. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8 kJ•mol-1 |
13.表是元素周期表的一部分,其中列出10种元素在周期表中的位置.
根据表回答下列问题(用元素符号或者相应的化学式表示):
(1)这10种元素中,化学性质最不活泼的是Ar.
(2)这些元素的最高价氧化物对应的水化物中,最强酸与最强碱生成的盐是KClO4.
(3)②、③和④3种元素所形成简单离子的半径大小次序是K+>Ca2+>Mg2+.
(4)⑦元素氢化物在常温下跟②发生反应的离子方程式是2K+2H2O=2K++2OH-+H2↑.
(5)用电子式表示⑨与①元素形成化合物的过程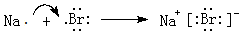 ,灼烧该化合物时,火焰呈黄 色.
,灼烧该化合物时,火焰呈黄 色.
(6)⑧元素和⑨元素两者的核电荷数之差是18,试举例说明⑧单质的氧化性比⑨单质强(用化学方程式表示)2KBr+Cl2=2KCl+Br2.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(1)这10种元素中,化学性质最不活泼的是Ar.
(2)这些元素的最高价氧化物对应的水化物中,最强酸与最强碱生成的盐是KClO4.
(3)②、③和④3种元素所形成简单离子的半径大小次序是K+>Ca2+>Mg2+.
(4)⑦元素氢化物在常温下跟②发生反应的离子方程式是2K+2H2O=2K++2OH-+H2↑.
(5)用电子式表示⑨与①元素形成化合物的过程
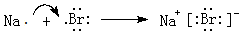 ,灼烧该化合物时,火焰呈黄 色.
,灼烧该化合物时,火焰呈黄 色.(6)⑧元素和⑨元素两者的核电荷数之差是18,试举例说明⑧单质的氧化性比⑨单质强(用化学方程式表示)2KBr+Cl2=2KCl+Br2.
10.通常人们把拆开1mol某化学键所吸收的能量或形成1mol某化学键所释放的能量看作该化学键的键能,键能的大小可用于估算化学反应的反应热(△H),已知
则下列热化学方程式不正确的是( )
| 化学键 | H-H | Cl-Cl | H-Cl |
| 键能 | 436kJ/mol | 243kJ/mol | 431kJ/mol |
| A. | $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)═HCl(g)△H=-91.5 kJ•mol-1 | |
| B. | H2(g)+Cl2(g)═2HCl(g)△H=-183 kJ•mol-1 | |
| C. | 2HCl(g)═H2(g)+Cl2(g)△H=183 kJ•mol-1 | |
| D. | $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)═HCl(g)△H=91.5 kJ•mol-1 |
11.设计下列实验方案鉴别Na2CO3和NaHCO3两种白色粉末,不能达到预期目的是( )
| A. | 分别向等量的白色粉末中加等体积、等浓度的稀盐酸,比较生成气体的快慢 | |
| B. | 分别向等质量的白色粉末中加等体积适量的水,比较固体溶解量的多少 | |
| C. | 分别配成溶液,加入澄清石灰水,比较是否有沉淀生成 | |
| D. | 分别将等质量的白色粉末加热,将产生的气体通入澄清石灰水中看是否变浑浊 |
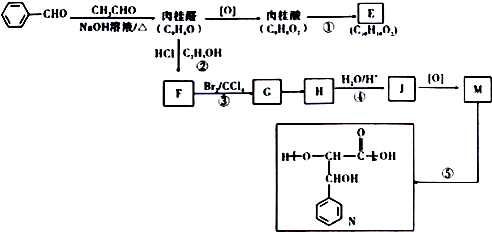
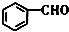 的名称是苯甲醛.
的名称是苯甲醛.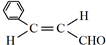 ,分子中最多有18个原子共平面.
,分子中最多有18个原子共平面. .
.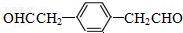 .
.