题目内容
18.下列反应的离子方程式书写正确的是( )| A. | NaHSO4溶液中加入Ba(OH)2溶液后恰好显中性Ba2++OH-+H++SO42-═BaSO4+H2O | |
| B. | 向澄清石灰水中通入过量CO2:OH-+CO2═HCO3- | |
| C. | 氢氧化钡溶液与稀 H2SO4 反应:Ba2++SO42-═BaSO4↓ | |
| D. | 碳酸钙与盐酸反应:CO32-+2H+═H2O+CO2↑ |
分析 A.反应后溶液呈中性,则硫酸氢钠与氢氧化钡按照物质的量2:1反应;
B.二氧化碳过量,反应生成碳酸氢钙;
C.漏掉了氢离子与氢氧根离子生成水的反应;
D.碳酸钙为难溶物,离子方程式中需要保留化学式.
解答 解:A.NaHSO4溶液中加入Ba(OH)2溶液后恰好显中性,氢离子与氢氧根离子恰好反应,正确的离子方程式为:Ba2++2OH-+2H++SO42-═BaSO4+2H2O,故A错误;
B.向澄清石灰水中通入过量CO2,反应的离子方程式为:OH-+CO2═HCO3-,故B正确;
C.氢氧化钡与稀硫酸反应生成硫酸钡沉淀和水,正确的离子方程式为:Ba2++2OH-+2H++SO42-═BaSO4+2H2O,故C错误;
D.碳酸钙与盐酸反应生成氯化钙、二氧化碳气体和水,碳酸钙不能拆开,正确的离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,故D错误;
故选B.
点评 本题考查了离子方程式的书写判断,为高考的高频题,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列叙述不正确的是( )
| A. | 碳酸氢钠加热可以分解,因为升高温度利于熵增的方向自发进行 | |
| B. | 在温度、压强一定的条件下,自发反应总是向△G=△H-T△S<0的方向进行 | |
| C. | 水结冰的过程不能自发进行的原因是熵减的过程,改变条件也不可能自发进行 | |
| D. | 混乱度减小的吸热反应一定不能自发进行 |
9.假如你是卫生防疫人员,为配制0.01mol•L-1的KMnO4消毒液,下列操作导致所配溶液浓度偏高的是( )
| A. | 称量时,左盘高,右盘低 | |
| B. | 定溶时俯视容量瓶刻度线 | |
| C. | 原容量瓶洗净后未干燥 | |
| D. | 摇匀后见液面下降,再加水至刻度线 |
13.对下列装置或操作描述正确的是( )
| A. | 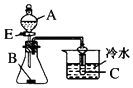 图中若A为醋酸,B为贝壳,C为苯酚钠溶液,则可验证醋酸的酸性大于碳酸,但不能验证碳酸的酸性大于苯酚 | |
| B. | 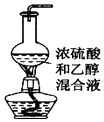 图用于实验室制乙烯 | |
| C. |  图用于实验室制乙炔并验证乙炔可以发生氧化反应 | |
| D. | 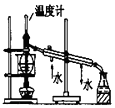 图用于实验室中分馏石油 |
10.下列说法不正确的是( )
| A. | 复分解反应一定不是氧化还原反应 | B. | 置换反应一定是氧化还原反应 | ||
| C. | 化合反应一定是氧化还原反应 | D. | 分解反应不一定是氧化还原反应 |
7.对于某些离子的检验及结论一定正确的是( )
| A. | 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,推断溶液中含有NH4+ | |
| B. | 无色试液在焰色反应中呈黄色,推断试液是钠盐溶液,不含钾盐 | |
| C. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,推断溶液中含有CO32- | |
| D. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,推断溶液中含有SO42- |