题目内容
反应4NH3(g)+5O2(g)=4NO(g)+6H2O(g)在 5L密闭容器中进行,30秒后,NO的物质的量增加了0.3mol,则此反应的平均速率v(x)(表示反应物的消耗速率或生成物的生成速率)为( )
| A、v (O2)=0.0l mol?L-1?s-1 |
| B、v (NO)=0.001 mol?L-1?s-1 |
| C、v (NH3)=0.001 mol?L-1?s-1 |
| D、v (H2O)=0.003 mol?L-1?s-1 |
考点:化学反应速率和化学计量数的关系
专题:化学反应速率专题
分析:根据n=
计算v(NO),再利用不同物质表示的速率之比等于其化学计量数之比计算.
| ||
| △t |
解答:
解:在 5L密闭容器中进行,30秒后,NO的物质的量增加了0.3mol,则v(NO)=
=0.002 mol?L-1?s-1,
A.v (O2)=
v(NO)=
×0.002 mol?L-1?s-1=0.0025 mol?L-1?s-1,故A错误;
B.由上述计算可知,v(NO)=
=0.002 mol?L-1?s-1,故B错误;
C.v (NH3)=v(NO)=0.002 mol?L-1?s-1,故C错误;
D.v (H2O)=
×0.002 mol?L-1?s-1=0.003 mol?L-1?s-1,故D正确,
故选D.
| ||
| 30s |
A.v (O2)=
| 5 |
| 4 |
| 5 |
| 4 |
B.由上述计算可知,v(NO)=
| ||
| 30s |
C.v (NH3)=v(NO)=0.002 mol?L-1?s-1,故C错误;
D.v (H2O)=
| 6 |
| 4 |
故选D.
点评:本题考查化学反应速率有关计算,难度不大,注意根据反应速率定义式理解化学反应速率规律.

练习册系列答案
相关题目
制取一氯乙烷最好采用的方法是( )
| A、乙烷和氯气反应 |
| B、乙烯和氯气反应 |
| C、乙烯和氯化氢反应 |
| D、乙烯和氯气、氢气反应 |
化学无处不在,下列与化学有关说法正确的是( )
| A、中性溶液的PH都相等 | ||||
| B、新型净水材料高铁酸钠是生产自来水理想的净水剂和杀菌剂 | ||||
C、
| ||||
| D、△H<0,△S<0的化学反应不能自发进行 |
NA表示阿伏伽德罗常数的数值,下列说法不正确的是( )
| A、将1molNH4NO3溶于一定浓度的稀氨水中,溶液呈中性,若不考虑挥发,溶液中一定含有NA个NH4 |
| B、1mol/LCH3COOH与1mol/L CH3COONa溶液等体积混合,溶液中CH3COOH和CH3COO-的总数为2NA |
| C、常温常压下,3.6g H2O中含有电子数为2NA |
| D、含有2NA个氧原子的氧气与臭氧的混合气体的质量为32g |
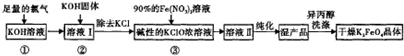
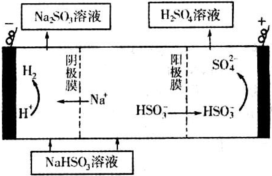 某科研小组为治理SO2对大气的污染,利用烟气中的SO2为原料制取硫酸.
某科研小组为治理SO2对大气的污染,利用烟气中的SO2为原料制取硫酸.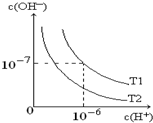 如图是在温度T1、T2时溶液中c(H+)、c(OH-)变化关系图,试回答:
如图是在温度T1、T2时溶液中c(H+)、c(OH-)变化关系图,试回答: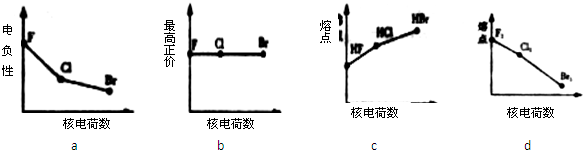
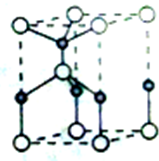 利用“卤化硼法”合成含B和N两种元素的功能陶瓷,下图为其晶胞结构示意图,则每个晶胞中含有B原子的个数为
利用“卤化硼法”合成含B和N两种元素的功能陶瓷,下图为其晶胞结构示意图,则每个晶胞中含有B原子的个数为