题目内容
制取一氯乙烷最好采用的方法是( )
| A、乙烷和氯气反应 |
| B、乙烯和氯气反应 |
| C、乙烯和氯化氢反应 |
| D、乙烯和氯气、氢气反应 |
考点:卤代烃简介,有机化学反应的综合应用
专题:有机反应
分析:根据反应产物及“原子经济”的理念分析,最理想的“原子经济”就是反应物的原子全部转化为期望的最终产物,这时原子的利用率为100%.
解答:
解:A、CH3CH3+Cl2→CH3CH2Cl+HCl,该反应有杂质HCl生成,且生成的氯代烃除氯乙烷外还有其它氯代烃,不符合原子经济的理念,故A错误;
B、CH2═CH2+Cl2→CH2ClCH2Cl,产物是二氯乙烷不是氯乙烷,故B错误;
C、CH2═CH2+HCl→CH3CH2Cl,生成物只有氯乙烷,符合原子经济理念,故C正确;
D、乙烯和氢气加成生成乙烷,乙烷和氯气反应有副产物HCl生成,不符合原子经济的理念,故D错误.
故选C.
B、CH2═CH2+Cl2→CH2ClCH2Cl,产物是二氯乙烷不是氯乙烷,故B错误;
C、CH2═CH2+HCl→CH3CH2Cl,生成物只有氯乙烷,符合原子经济理念,故C正确;
D、乙烯和氢气加成生成乙烷,乙烷和氯气反应有副产物HCl生成,不符合原子经济的理念,故D错误.
故选C.
点评:本题考查了乙烯和乙烷的化学性质,难度不大,注意烷烃和烯烃化学性质的区别.

练习册系列答案
相关题目
金属单质与足量Cl2反应后,生成物的化学式中,不正确的是( )
| A、FeCl2 |
| B、AlCl3 |
| C、MgCl2 |
| D、CuCl2 |
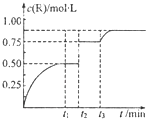 一定温度下,将1molN气体充入2L恒容密闭容器中,发生反应:M(g)+N(g)?xR(g)+Q(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体R的浓度随时间变化如图所示.下列说法正确的是( )
一定温度下,将1molN气体充入2L恒容密闭容器中,发生反应:M(g)+N(g)?xR(g)+Q(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体R的浓度随时间变化如图所示.下列说法正确的是( )| A、该反应方程式中:x=1 |
| B、t1~t3间该反应的平衡常系数均为4 |
| C、t2时刻改变的条件是使用催化剂 |
| D、t3时刻改变的条件是移去少量Q |
已知2Cu(NO3)2
2CuO+4NO2↑+O2↑;已知带火星的木条在空气中不能复燃,但伸进分解产生的混合气体中,木条能复燃,分析说明( )
| ||
| A、NO2具有氧化性 |
| B、NO2具有还原性 |
| C、NO2不发生反应 |
| D、只有O2才能燃烧 |
将11.2g的MgCu混合物完全溶解于足量的硝酸中,收集反应产生的X气体.再向所得溶液中加入适量的氢氧化钠溶液,产生21.4g沉淀.根据题意推断气体X的成分可能是( )
| A、0.3 mol NO2和0.3 mol NO |
| B、0.1 mol NO、0.2 mol NO2和0.05 mol N2O4 |
| C、0.2 mol NO2和0.1 mol N2O4 |
| D、0.6 mol NO |
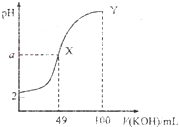 常温下向100mL0.1mol?L-1HA溶液中逐滴加入0.2mol?L-1KOH溶液,图中所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计),已知X点溶液呈中性.下列说法中,不正确的是( )
常温下向100mL0.1mol?L-1HA溶液中逐滴加入0.2mol?L-1KOH溶液,图中所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计),已知X点溶液呈中性.下列说法中,不正确的是( )| A、HA为一元弱酸 |
| B、X点溶液的温度高于Y点 |
| C、X点水的电离程度大于Y点水的电离程度 |
| D、Y点对应点的溶液中c(K+)>c(A-)>c(OH-) |
碳原子数小于或等于8的单烯烃,与HBr加成反应的产物只有一种结构,符合条件的单烯烃(不考虑反异构和立体异构)( )
| A、4种 | B、5种 | C、6种 | D、7种 |
反应4NH3(g)+5O2(g)=4NO(g)+6H2O(g)在 5L密闭容器中进行,30秒后,NO的物质的量增加了0.3mol,则此反应的平均速率v(x)(表示反应物的消耗速率或生成物的生成速率)为( )
| A、v (O2)=0.0l mol?L-1?s-1 |
| B、v (NO)=0.001 mol?L-1?s-1 |
| C、v (NH3)=0.001 mol?L-1?s-1 |
| D、v (H2O)=0.003 mol?L-1?s-1 |
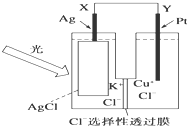 一种光化学电池的结构如图,当光照在表面涂有氯化银的银片上时,AgCl(s)
一种光化学电池的结构如图,当光照在表面涂有氯化银的银片上时,AgCl(s)