题目内容
4.下列对实验现象的预测与实际相符的是( )| 选项 | 实验 | 预测现象 |
| A | 将SO2通入紫色石蕊溶液中 | 石蕊溶液先变红后褪色 |
| B | 将CO2气体通入足量的CaCl2溶液中 | 产生白色沉淀 |
| C | 常温下,将用砂纸打磨过的铝片投入浓硫酸中 | 产生刺激性气体 |
| D | 将酸性高锰酸钾溶液滴入足量的乙醇中 | 高锰酸钾溶液褪色 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.二氧化硫为酸性氧化物漂白性具有选择性,在石蕊试液中只显示酸性;
B.二氧化碳和氯化钙溶液不发生反应;
C.常温下铝在浓硫酸中发生钝化不能继续反应;
D.乙醇被高锰酸钾溶液氧化.
解答 解:A.将SO2通入紫色石蕊溶液中石蕊溶液先变红,故A错误;
B.盐酸酸性大于碳酸,将CO2气体通入足量的CaCl2溶液中不发生反应,无沉淀生成,故B错误;
C.常温下,将用砂纸打磨过的铝片投入浓硫酸中发生钝化不能继续反应,无刺激性气体,故C错误;
D.将足量乙醇通入酸性高锰酸钾溶液中,溶液褪色,是因为高锰酸钾是强氧化剂,通入乙醇会被氧化,本身被还原为无色的锰离子,故D正确;
故选D.
点评 本题考查了物质性质分析、物质特征性质的理解应用,掌握基础是解题关键,题目难度中等.

练习册系列答案
相关题目
19.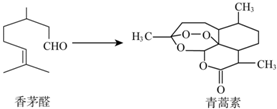 中国科学家屠呦呦因为创制了新型抗疟疾-青蒿素,获得2015年诺贝尔奖.青蒿素可由香茅醛为原料制取,下列说法错误的是( )
中国科学家屠呦呦因为创制了新型抗疟疾-青蒿素,获得2015年诺贝尔奖.青蒿素可由香茅醛为原料制取,下列说法错误的是( )
 中国科学家屠呦呦因为创制了新型抗疟疾-青蒿素,获得2015年诺贝尔奖.青蒿素可由香茅醛为原料制取,下列说法错误的是( )
中国科学家屠呦呦因为创制了新型抗疟疾-青蒿素,获得2015年诺贝尔奖.青蒿素可由香茅醛为原料制取,下列说法错误的是( )| A. | 香茅醛能使Br2的CCl4溶液褪色 | B. | 青蒿素分子式为C15H22O5 | ||
| C. | 青蒿素含有和H2O2相同的过氧键 | D. | 青蒿素能与氢气发生加成反应 |
16. 常温下,向25 mL 0.1ml•L-1NaOH溶液中逐滴加入 0.1 mo1•L-1CH3C00H溶液,曲线如图所示,有关粒子浓度关系正确的是( )
常温下,向25 mL 0.1ml•L-1NaOH溶液中逐滴加入 0.1 mo1•L-1CH3C00H溶液,曲线如图所示,有关粒子浓度关系正确的是( )
 常温下,向25 mL 0.1ml•L-1NaOH溶液中逐滴加入 0.1 mo1•L-1CH3C00H溶液,曲线如图所示,有关粒子浓度关系正确的是( )
常温下,向25 mL 0.1ml•L-1NaOH溶液中逐滴加入 0.1 mo1•L-1CH3C00H溶液,曲线如图所示,有关粒子浓度关系正确的是( )| A. | 曲线上任一点:c(Na+)+c(H+)=c(0H-)+c(CH3C00H) | |
| B. | 在 B点,a=25,且有 c(Na+)=c(CH3C00-)>c(0H-)=c(H+) | |
| C. | 在C点:c(Na+)>c(CH3C00-)>c(H+)>c(0H-) | |
| D. | 在D点:c(CH3C00-)+c(CH3C00H)=2c(Na+) |
13.在厨房里对水进行下列操作,能促进水的电离的是( )
| A. | 加入少量酒精 | B. | 加入少量食醋 | ||
| C. | 把水放入冰箱中使其降温至1℃ | D. | 把水加热至沸腾 |
14.有A、B、C、D四种金属,投入水中只有C反应放出氢气,将A投入D的盐溶液中可置换出金属D,B的最高价氧化物的水化物碱性比A的最高价氧化物的水化物碱性强,则四种金属的金属性强弱顺序正确的是( )
| A. | A>B>C>D | B. | D>B>A>C | C. | B>A>C>D | D. | C>B>A>D |
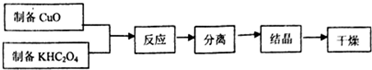
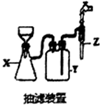
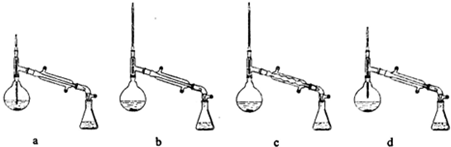
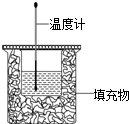 50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程 中放出的热量可计算中和热.回答下列问题:
50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程 中放出的热量可计算中和热.回答下列问题: