题目内容
14.有A、B、C、D四种金属,投入水中只有C反应放出氢气,将A投入D的盐溶液中可置换出金属D,B的最高价氧化物的水化物碱性比A的最高价氧化物的水化物碱性强,则四种金属的金属性强弱顺序正确的是( )| A. | A>B>C>D | B. | D>B>A>C | C. | B>A>C>D | D. | C>B>A>D |
分析 金属的金属性越强,其单质与酸或水反应生成氢气越容易,其最高价氧化物的水化物碱性越强;较活泼的金属能置换出较不活泼金属,据此判断金属性强弱.
解答 解:A、B、C、D四种金属,投入水中只有C反应放出氢气,说明C金属性很强;
将A投入D的盐溶液中可置换出金属D,说明金属性A>D;
B的最高价氧化物的水化物碱性比A的最高价氧化物的水化物碱性强,说明金属性B>A;
所以金属性强弱顺序是:C>B>A>D,
故选D.
点评 本题考查金属的金属性强弱判断,题目难度不大,金属的金属性强弱判断方法有:金属与酸或水反应生成氢气难易程度、其最高价氧化物的水化物碱性强弱、金属之间的置换反应等,注意不能根据失电子多少判断金属性强弱,要根据失电子难易程度判断金属性强弱,试题培养了学生的灵活应用能力.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案
相关题目
4.下列对实验现象的预测与实际相符的是( )
| 选项 | 实验 | 预测现象 |
| A | 将SO2通入紫色石蕊溶液中 | 石蕊溶液先变红后褪色 |
| B | 将CO2气体通入足量的CaCl2溶液中 | 产生白色沉淀 |
| C | 常温下,将用砂纸打磨过的铝片投入浓硫酸中 | 产生刺激性气体 |
| D | 将酸性高锰酸钾溶液滴入足量的乙醇中 | 高锰酸钾溶液褪色 |
| A. | A | B. | B | C. | C | D. | D |
2.25℃时,已知Ksp(Ag2SO4)=1.2×10-5,Ksp(AgCl)=1.8×10-10,Ksp(Ag2C2O4)=3.5×10-11,Ksp(AgI)=1.5×10-16,该温度下有关叙述正确的是( )
| A. | AgCl、Ag2C2O4、AgI三者的饱和溶液中c(Ag+)大小顺序:Ag2C2O4>AgCl>AgI | |
| B. | 将0.02mol•L-1AgNO3溶液和0.02mol•L-1Na2SO4溶液等体积混合,有沉淀生成 | |
| C. | 向5mL饱和AgCl溶液中滴加0.5mL0.1mol•L-1KI溶液,无沉淀生成 | |
| D. | 向浓度均为0.1mol•L-1NaCl和KI混合溶液中滴加AgNO3溶液,先有白色沉淀生成 |
19.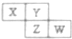 X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法正确的是( )
 X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法正确的是( )| A. | X的气态氧化物比Y的稳定 | |
| B. | X与Y形成的化合物都易溶于水 | |
| C. | Z与Y只能形成ZY3型化合物 | |
| D. | W的最高价氧化物对应水化物的酸性比Z的强 |
3.毒奶粉主要是奶粉中含有有毒的三聚氰胺(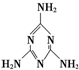 ).下列关于三聚氰胺分子的说法中正确的是( )
).下列关于三聚氰胺分子的说法中正确的是( )
 ).下列关于三聚氰胺分子的说法中正确的是( )
).下列关于三聚氰胺分子的说法中正确的是( )| A. | 所有氮原子均采取sp3杂化 | |
| B. | 一个三聚氰胺分子中共含有15个σ键 | |
| C. | 属于极性分子 | |
| D. | 三聚氰胺分子中同时含有极性键和非极性键 |
4.下列有机物的命名正确的是( )
| A. | 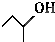 2-甲基-1-丙醇 2-甲基-1-丙醇 | B. | 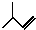 2-甲基-3-丁烯 2-甲基-3-丁烯 | ||
| C. |  2-甲基戊烷 2-甲基戊烷 | D. | 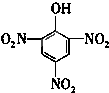 1,3,5-三硝基苯酚 1,3,5-三硝基苯酚 |
 如图所示,把试管放入盛有25度时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再滴入5mL盐酸,试回答下列问题.
如图所示,把试管放入盛有25度时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再滴入5mL盐酸,试回答下列问题.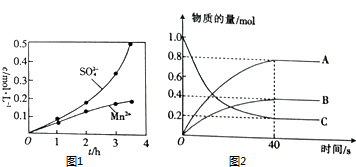 硫及其化合物在药物、造纸、炸药及石油加工等方面具有广泛应用.回答下列问题:
硫及其化合物在药物、造纸、炸药及石油加工等方面具有广泛应用.回答下列问题: