题目内容
15.二草酸合铜(Ⅱ)酸钾晶体{K2[Cu(C2O4)2]•2H2O}制备流程下: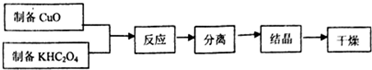
(已知:H2C2O4 $\frac{\underline{\;\;△\;\;}}{\;}$CO↑+CO2↑+H20)
(1)制备CuO:向CuSO4溶液中滴入NaOH溶液,加热煮沸,冷却,用如图所示的装置抽滤,然后用蒸馏水洗涤氧化铜.
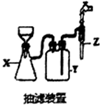
①抽滤装置中仪器Z接在水龙头上,其作用是起抽气的作用,使吸滤瓶中的压强减小.
②用蒸馏水洗涤氧化铜时,证明已洗涤干净的方法是:取最后一次洗涤滤液,滴入BaCl2溶液,若无白色沉淀,说明已洗涤干净.
(2)制取KHC2O4,将H2C2O4晶体加入蒸馏水中,微热,溶解过程中温度不能太高,原因是温度过高,草酸会分解,充分溶解后分数次加入K2CO3,反应生成KHC2O4,将滤纸上的CuO充分转移到热的KHC2O4溶液中,以下操作方案中合理的是AD(填序号)
A.剪碎滤纸,加入到热的KHC2O4溶液中,待充分反应后趁热过滤
B.用稀硫酸溶解滤纸上的氧化铜,然后将溶液转入热的KHC2O4溶液中
C.用氢氧化钾溶液溶解氧化铜,并转入热的KHC2O4溶液中
D.在空气中灼烧滤纸,将剩余的固体转入热的KHC2O4溶液
(3)将CuO与KHC2O4混合液在50℃水浴加热至反应充分,发生反应的化学方程式为2KHC2O4+CuO$\frac{\underline{\;50℃\;}}{\;}$K2[Cu(C2O4)2]+H2O;
(4)二草酸合铜(Ⅱ)酸钾晶体的制备也可以用CuSO4晶体和K2C2O4溶液反应得到.从硫酸铜溶液中获得硫酸铜晶体的实验步骤为:加入适量乙醇,蒸发浓缩,冷却结晶,过滤,洗涤,干燥.
①加入适量乙醇的优点有:
a、缩短加热的时间,降低能耗;
b、降低硫酸铜的溶解度,有利于硫酸铜晶体析出.
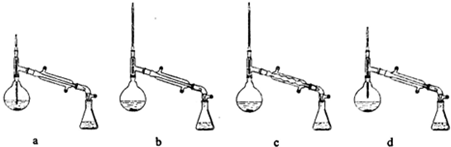
②在蒸发浓缩的初始阶段为了将乙醇回收,采用了蒸馏操作,下列装置中仪器选择及安装都正确的是b(填序号).
分析 (1)①根据抽滤的原理可知,将抽滤装置中仪器Z接在水龙头上,可以起抽气的作用,使吸滤瓶中的压强减小,从而达到抽滤的目的;
②CuO表面会附着硫酸根离子,用氯化钡溶液检验最后一次洗涤液中是否含有硫酸根离子判断是否洗涤干净;
(2)H2C2O4晶体加入蒸馏水中,温度过高,草酸会分解;过滤时滤纸上沾有大量的氧化铜固体,所以应直接将洗涤干净的氧化铜固体连同滤纸一起加入到草酸氢钾溶液中,充分反应后取出滤纸或将滤纸灼烧成灰再将剩余的固体转入热的KHC2O4溶液;
(3)CuO与KHC2O4溶液在50℃水浴加热条件下反应生成K2[Cu(C2O4)2]与H2O;
(4)从硫酸铜溶液中获得硫酸铜晶体时,为减少硫酸铜的溶解,可用加入少量乙醇,并用蒸馏的方法分离乙醇,根据蒸馏装置选择仪器;
解答 解:(1)①根据抽滤的原理可知,将抽滤装置中仪器Z接在水龙头上,可以起抽气的作用,使吸滤瓶中的压强减小,从而达到抽滤的目的,
故答案为:起抽气的作用,使吸滤瓶中的压强减小;
②CuO表面会附着硫酸根离子,检验是否洗涤干净的具体方法是:取最后一次洗涤滤液,滴入BaCl2溶液,若无白色沉淀,说明已洗涤干净,
故答案为:取最后一次洗涤滤液,滴入BaCl2溶液,若无白色沉淀,说明已洗涤干净;
(2)H2C2O4晶体加入蒸馏水中,温度过高,草酸会分解;过滤时滤纸上沾有大量的氧化铜固体,所以应直接将洗涤干净的氧化铜固体连同滤纸一起加入到草酸氢钾溶液中,充分反应后取出滤纸或将滤纸灼烧成灰再将剩余的固体转入热的KHC2O4溶液,故选AD,
故答案为:温度过高,草酸会分解;AD;
(3)根据题意可知,CuO与KHC2O4溶液在50℃水浴加热条件下反应生成K2[Cu(C2O4)2]与H2O,反应的方程式为:2KHC2O4+CuO$\frac{\underline{\;50℃\;}}{\;}$K2[Cu(C2O4)2]+H2O,
故答案为:2KHC2O4+CuO$\frac{\underline{\;50℃\;}}{\;}$K2[Cu(C2O4)2]+H2O;
(4)①从硫酸铜溶液中获得硫酸铜晶体时,为减少硫酸铜的溶解,降低硫酸铜的溶解度,有利于硫酸铜晶体析出,可用加入少量乙醇,
故答案为:降低硫酸铜的溶解度,有利于硫酸铜晶体析出;
②在蒸发浓缩的初始阶段还采用了蒸馏的方法,可起到回收乙醇的作用,根据蒸馏装置的要求可知,ad图中温度计的位置都有错,c图中用球形冷凝管错,故答案为:b.
点评 本题考查物质的制备,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质以及实验的原理和操作,难度不大.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案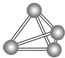 意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4气体分子.N4分子结构如图所示,下列说法正确的是( )
意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4气体分子.N4分子结构如图所示,下列说法正确的是( )| A. | N4分子属于一种新型的化合物 | B. | N4分子中只含有共价键 | ||
| C. | 1 mol N4分子所含共价键数为4NA | D. | N4沸点比P4(白磷)高 |
| A. | 已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol,则浓硫酸与稀NaOH溶液反应、稀醋酸与稀NaOH溶液反应所测得的中和热都为△H=-57.3kJ/mol | |
| B. | 由C(石墨,s)═C(金刚石,s)△H=+1.9kJ/mol,可知金刚石比石墨稳定 | |
| C. | 在用标准盐酸滴定未知浓度氢氧化钠溶液的实验中,若用待测液润洗锥形瓶,则测定结果偏低(其他操作正确) | |
| D. | 向存在着FeCl3 (黄色)+3KSCN?Fe(SCN)3(血红色)+3KCl平衡体系的溶液中,加少量KCl固体,溶液血红色不发生变化 |
| 分子式 | 外观 | 热分解温度 | 熔点 | 溶解性 |
| CO(NH2)2•H2O2 | 白色晶体 | 45℃ | 75~85℃ | 易溶于水、有机溶剂 |
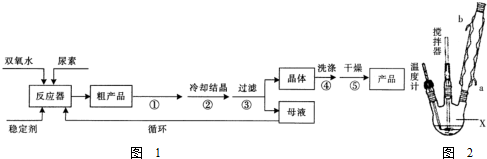
请回答下列问题:
(1)仪器X的名称是三颈烧瓶;冷凝管中冷却水从b(填“a”或“b”)口出来;
(2)该反应的温度控制30℃而不能过高的原因是防止双氧水和过氧化尿素分解.
(3)搅拌器是否可用铁质材料否(填“是”或“否”),原因是铁和双氧水反应生成铁离子,促进双氧水分解;
(4)步骤①宜采用的操作是C.
A.加热蒸发 B.常压蒸发 C.减压蒸发
(5)若实验室制得少量该晶体,过滤后需要用冷水洗涤,具体的洗涤操作是沿玻璃棒注入蒸馏水至浸没晶体表面,静置待水自然流下,重复操作2-3次.
(6)准确称取1.000g产品于250mL锥形瓶中,加适量蒸馏水溶解,再加2mL6mol•L-1H2SO4,用0.2000mol•L-1KMnO4标准溶液滴定至终点时消耗18.00mL(尿素与KMnO4溶液不反应),则产品中CO(NH2)2•H2O2的质量分数为84.6%;若滴定后俯视读数,则测得的过氧化尿素含量偏低(填“偏高”、“偏低”或“不变”).
| A. | 位于周期表中同一周期的元素,原子具有相同的电子层数 | |
| B. | 凡是位于周期表中同一主族的元素,原子具有相同的最外层电子数 | |
| C. | 凡是位于周期表中同一周期的元素,都是按从左到右的顺序原子核外最外层电子数由1递增至8 | |
| D. | 凡是位于周期表中同一主族的元素,都是按从上到下的顺序原子核外电子层数逐渐递增 |
| 选项 | 实验 | 预测现象 |
| A | 将SO2通入紫色石蕊溶液中 | 石蕊溶液先变红后褪色 |
| B | 将CO2气体通入足量的CaCl2溶液中 | 产生白色沉淀 |
| C | 常温下,将用砂纸打磨过的铝片投入浓硫酸中 | 产生刺激性气体 |
| D | 将酸性高锰酸钾溶液滴入足量的乙醇中 | 高锰酸钾溶液褪色 |
| A. | A | B. | B | C. | C | D. | D |
 如图所示,把试管放入盛有25度时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再滴入5mL盐酸,试回答下列问题.
如图所示,把试管放入盛有25度时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再滴入5mL盐酸,试回答下列问题.