��Ŀ����
15��ij�о�С����ij2L�ܱ������м���һ�����Ĺ���A������B��������ӦA��s��+2B��g��?D��g��+E��g����H=QkJ•mol-1����T1��ʱ����Ӧ���е���ͬʱ���ø����ʵ����ʵ��������| ʱ�䣨min�� ���ʵ�����mol�� | 0 | 10 | 20 | 30 | 40 | 50 |
| B | 2.00 | 1.36 | 1.00 | 1.00 | 1.20 | 1.20 |
| D | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
| E | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
��2��30min��ֻ�ı�ijһ��������Ӧ���´ﵽƽ�⣬���ݱ��е������жϸı������������ae������ĸ��ţ���
a��ͨ��һ������B�� b������һ�����Ĺ���A�� c���ʵ���С���������
d�����߷�Ӧ��ϵ�¶ȡ� e��ͬʱ����0.2molB��0.1molD��0.1molE
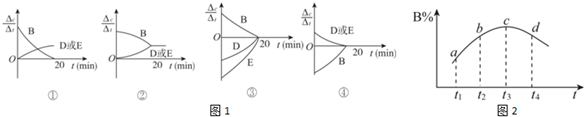
��3�����ڸ÷�Ӧ���ø����ʱ�ʾ�ķ�Ӧ������ʱ��Ĺ�ϵʾ������Ϊͼ1�еĢܣ�����ţ���
��4��ά��������������¶�T1���䣬����������м���1.60 mol B��0.20 mol D��0.20 mol E��nmolA���ﵽƽ����������20����ʱ�����ʵ�Ũ����ȫ��ͬʱ����Ͷ�����A�����ʵ���n��ȡֵ��Χ�ǣ�0.3��
��5��ά��������������¶�T1���䣬�����ʵ���ʼ���ʵ���Ϊn��A��=1.0 mol��n��B��=3.0 mol��n��D��=a mol���ﵽƽ���n��E��=0.50 mol����a=1.5��
��6�������ܱ��������ȣ�ʵ����B��ת����B%��ʱ��仯��ʾ��ͼ��ͼ2��ʾ����ͼ��֪��QС��0������ڡ���С�ڡ�����c��v������v��������ڡ���С�ڡ����ڡ�����
���� ��1��T1��ʱ��20min��40min����ƽ�⣬�ɸ��ݸ����ʵ�Ũ�ȼ�����¶���ƽ�ⳣ����
��2��30min���ɱ������ݿ�֪��Ӧ��ϵ��Ӧ�������������ʵ��������ӣ�
��3�����ݻ�ѧ��Ӧ�ﵽƽ��Ĺ��̷����ͷ�Ӧ���ʱ仯�жϣ��ﵽƽ��״̬��Ӧ�ǿ��淴Ӧ�����淴Ӧ������ͬ������֮�ȵ��ڻ�ѧ����ʽ������֮�ȣ�
��4�����ṩ�����ݿ�֪���������20����ʱ�����ʵ�Ũ����ȫ��ͬʱ����������D��E����Ϊ0.5-0.2=0.3mol��A����Ҫ��ת������A������С��0.3mol��
��5��������ʽ���B��D��Eƽ�����ʵ����ֱ�Ϊ2mol����a+0.5��mol��0.5mol������K=0.25�����a��ֵ��
��6����ߵ��ƽ��״̬���¶�����B��ת���ʼ�С����������Ӧ�Ƿ��ȷ�Ӧ��
��� �⣺��1���ɱ���֪40���Ӵ�ƽ��״̬�����ƽ��Ũ�Ⱥ�ƽ�ⳣ��������㣬����K=$\frac{\frac{0.6}{2}��\frac{0.6}{2}}{\frac{1.2}{2}��\frac{1.2}{2}}$=0.25���ʴ�Ϊ��0.25��
��2��30nim��BDE�����ӣ���ͼ��֪��Ӧ��ϵ��Ӧ�������������ʵ��������ӣ���������Ӧ��B������ƽ�������ƶ������·�Ӧ������ɵ����ʵ��������ӣ��仯��ͬʱ�ı䷴Ӧ��������
a��ͨ��һ������Bƽ��������У�BDE����a���ϣ���������������
b������һ�����Ĺ���A��Ӱ��ƽ���ƶ���BDE���䣬��b�����ϣ�
c����Ӧǰ������������䣬�ʵ���С�����������ƽ�ⲻ������c�����ϣ�����������
d����Ӧ�����ȷ�Ӧ�����߷�Ӧ��ϵ�¶ȣ�ƽ��������У�B��С����d�����ϣ�
e��ͬʱ����0.2molB��0.1molD��0.1molE��BDEŨ������e���ϣ�
��ѡ��ae��
��3��A��s��+2B��g��?D��g��+E��g����H=QkJ•mol-1����Ӧǰ������������䣻
��B�ķ�Ӧ���ʲ���Ϊ0��
��B�ķ�Ӧ���ʺ�DE��Ӧ���ʴﵽƽ��״̬������ͬ��
��DE�仯���� ��ͬ��ͼ����
��DE������ͬ��ͼ���ʾ����������У�B��Ӧ��������DE��Ӧ���ʼ�С���ʢ���ȷ
�ʴ�Ϊ���ܣ�
��4�����ṩ�����ݿ�֪���������20����ʱ�����ʵ�Ũ����ȫ��ͬʱ����������D��E����Ϊ0.5-0.2=0.3mol��A����Ҫ��ת������A������С��0.3mol�����淴Ӧ������ȫ���У�A���ǹ��壬��Ҳ����ʣ�࣬����A�����ʵ���nȡֵ��Χ����0.3mol��
�ʴ�Ϊ����0.3��
��5��A��s��+2B��g��?D��g��+E��g��
��ʼ�� 3.0mol amol 0mol
ƽ���� 3-0.5��2 a+0.50 0.50mol
$\frac{\frac{0.5}{2}��\frac{a+0.5}{2}}{\frac{2}{2}��\frac{2}{2}}$
=0.25�����a=1.5���ʴ�Ϊ��1.5��
��6����ߵ��ƽ��״̬���¶�����B��ת���ʼ�С����������Ӧ�Ƿ��ȷ�Ӧ����QС��0��c��Ϊƽ��״̬�����淴Ӧ������ȣ��ʴ�Ϊ��С�ڣ����ڣ�
���� �����ۺϿ��黯ѧƽ���Ӱ�����أ���ѧƽ��ļ������жϣ�Ϊ�߿��������ͺ�Ƶ���㣬ע�����ͼ��ķ������жϣ��ѶȲ���

 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�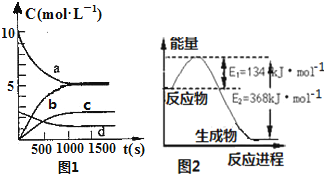 ���ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���ã����ٵ����������ڴ����е��ŷ��ǻ�����������Ҫ����֮һ��
���ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���ã����ٵ����������ڴ����е��ŷ��ǻ�����������Ҫ����֮һ����1��һ���¶��£������Ϊ2L�ĺ����ܱ������г���20molNO2��5molO2�������·�Ӧ��4NO2��g��+O2��g��?2N2O5��g������֪��ϵ��n��NO2����ʱ��仯��ͼ1��
| t��s�� | 0 | 500 | 1000 | 1500 |
| n��NO2����mol�� | 20 | 13.96 | 10.08 | 10.08 |
�ڷ�Ӧ�ﵽƽ���NO2��ת����Ϊ����Ҫ����NO2��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��BC��
A���ٳ���NO2 B���ٳ���4molNO2��1molO2 C�������¶� D�����뺤��
��ͼ1�б�ʾN2O5��Ũ�ȵı仯������c��
��2��ͼ2��1molNO2�����1molCO���巴Ӧ����CO2�����NO��������������仯ʾ��ͼ������֪��
2NO��g��+2CO��g��?N2��g��+2CO2��g����H=-760.3kJ•mol-1����Ӧ��
N2��g��+2NO2��g��?4NO��g�� �ġ�H=+292.3kJ•mol-1��
| A�� | ��Ϊ�ʱ���ر䶼�뷴Ӧ���Է����йأ�����ʱ���ر�����Ե�����Ϊ��Ӧ�Է��Ե��о� | |
| B�� | �����ܹ��Է����е����ȷ�Ӧ����ԭ������ϵ���Է�������Ҷ����ӵķ���ת������� | |
| C�� | ��H��0����S��0�ķ�Ӧ���¶ȵ�ʱ�����Է����� | |
| D�� | ����������������������£�ʹ�ô��������Ըı仯ѧ��Ӧ���еķ��� |
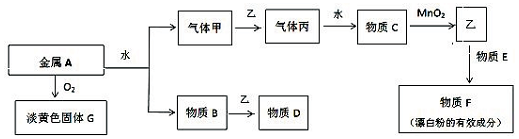
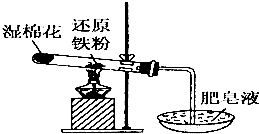 ������û����������ʱ������ˮ��������Ӧ���������£�����ˮ�����ܷ�Ӧ��С���������ʵ��̽��������ˮ������Ӧ���������
������û����������ʱ������ˮ��������Ӧ���������£�����ˮ�����ܷ�Ӧ��С���������ʵ��̽��������ˮ������Ӧ���������