题目内容
7.某气态烃A在标准状况下的密度为1.25g/L,其产量可以用来衡量一个国家的石油化工发展水平.B和D都是生活中常见的有机物,D能跟碳酸氢钠反应,F有香味.它们之间的转化关系如图1所示: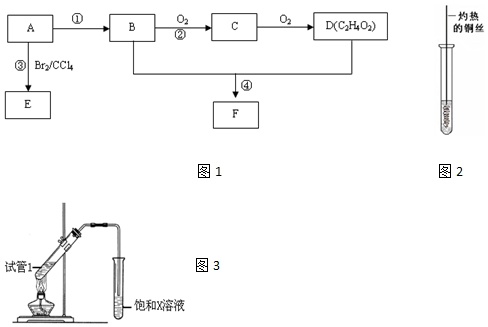
(1)A的结构简式为CH2=CH2,B中官能团的电子式为
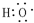 ,D中官能团为羧基(-COOH).
,D中官能团为羧基(-COOH).(2)反应①的反应类型是加成反应,反应③的化学方程式为CH2=CH2+Br2→CH2BrCH2Br.
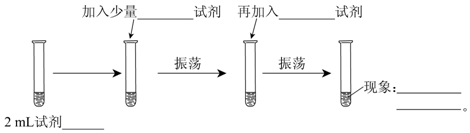
(3)反应②在Cu做催化剂的条件下进行,该实验的步骤是将红亮的铜丝置于酒精灯上加热,待铜丝变为黑色时,迅速将其插入到装有B的试管中(如图2所示).重复操作2-3次.该反应的化学方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
(4)C与新制Cu(OH)2反应的化学方程式:CH3CHO+2Cu(OH)2$\stackrel{△}{→}$CH3COOH+Cu2O↓+2H2O;
(5)B、D在浓硫酸的作用下实现反应④,实验装置如图3所示:试管1中装入药品后加热.图中X的化学式为Na2CO3.其作用是abd(填选项)
a.溶解挥发出的乙醇蒸汽.
b.使挥发出的乙酸被碳酸钠溶液反应.
c.吸收反应的尾气,防止挥发后污染空气.
d.饱和碳酸钠溶液能降低酯的溶解度,使其在上层析出.
试管1反应的化学方程式为CH3COOH+CH3CH2OH
 CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.
分析 气态烃A在标况下的密度为1.25g/L,其摩尔质量=1.25g/L×22.4L/mol=28g/mol,A是一种重要的化工原料,它的产量通常用来衡量一个国家石油化工水平,故A是乙烯,B和D都是生活中常见的有机物,乙烯和水发生加成反应生成B,则B是乙醇,乙醇和氧气反应生成C,则C是乙醛,C和氧气反应生成D,D是乙酸,乙醇和乙酸反应生成F为乙酸乙酯,A与溴发生加成反应生成1,2-二溴乙烷,以此来解答.
解答 解:(1)A是一种气态烃,在标准状况下的密度是1.25g/L,摩尔质量=1.25g/L×22.4L/mol=28g/mol,其产量是衡量一个国家石油化工发展水平,则A为CH2=CH2,A的结构简式为CH2=CH2,B氧化生成C、C氧化生成D,B和D都是生活中常见的有机物,结合D的分子式可知,B为CH3CH2OH,B中官能团的电子式为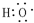 ,乙醇和氧气反应生成C,则C是乙醛,C和氧气反应生成D,D是乙酸,D中官能团的名称为羧基(-COOH),
,乙醇和氧气反应生成C,则C是乙醛,C和氧气反应生成D,D是乙酸,D中官能团的名称为羧基(-COOH),
故答案为:CH2=CH2;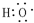 ;羧基(-COOH);
;羧基(-COOH);
(2)A为CH2=CH2,反应①为乙烯与水的加成反应,反应的化学方程式为:CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH,反应③是乙烯与溴发生加成反应生成1,2-二溴乙烷,反应方程式为:CH2=CH2+Br2→CH2BrCH2Br,
故答案为:加成反应;CH2=CH2+Br2→CH2BrCH2Br;
(3)B是乙醇,乙醇和氧气反应生成C,则C是乙醛,所以反应②的化学方程式为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
(4)C是乙醛,乙醛和新制Cu(OH)2的反应发生氧化反应,乙醛分子中的醛基被氧化为羧基,氢氧化铜被还原为氧化亚铜红色沉淀:CH3CHO+2Cu(OH)2$\stackrel{△}{→}$CH3COOH+Cu2O↓+2H2O,
故答案为:CH3CHO+2Cu(OH)2$\stackrel{△}{→}$CH3COOH+Cu2O↓+2H2O;
(5)B、D在浓硫酸的作用下实现反应④,B为CH3CH2OH,D是乙酸,在乙酸乙酯的制备实验中,用饱和的碳酸钠溶液吸收乙酸乙酯中的乙酸与乙醇,能溶解乙醇,吸收乙酸,2CH3COOH+CO32-→2CH3COO-+H2O+CO2↑,有利于乙酸乙酯的分层,所以X为Na2CO3,其作用是abd,反应④的化学方程式为:CH3COOH+CH3CH2OH  CH3COOCH2CH3+H2O,
CH3COOCH2CH3+H2O,
故答案为:Na2CO3;abd;CH3COOH+CH3CH2OH  CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.
点评 本题考查有机物推断,关键是掌握烯与醇、醛、羧酸的性质与转化,熟练掌握有机反应类型是解答关键,注意掌握常见有机物官能团及其性质,题目难度中等.

 计算高手系列答案
计算高手系列答案| A. | 0.5mol/L | B. | 5mol/L | C. | 10mol/L | D. | 20mol/L |
| A. | 乙烷 | B. | 乙醇 | C. | 乙酸 | D. | 苯 |
| A. | 氧化铝与盐酸反应:Al2O3+6H+═2Al3++3H2O | |
| B. | 氢氧化铝与NaOH溶液反应:Al(OH)3+OH-═AlO2-+2H2O | |
| C. | 向AlCl3溶液中滴加氨水:Al3++3OH-═Al(OH)3↓ | |
| D. | 向AlCl3溶液中加入过量NaOH溶液:Al3++4OH-═AlO2-+2H2O |
 无机化合物可根据其组成和性质进行分类
无机化合物可根据其组成和性质进行分类(1)如图所示的物质分类方法的名称是树状分类法.
(2)以Na、K、H、O、S、N中任两种或三种元素组成合适的物质,分别填在下表中②③⑥后面.
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①HCl②H2SO4 | ③NaOH ④Ba(OH)2 | ⑤Na2CO3 ⑥K2SO4 | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O2 |
(4)写出实验室由⑩制备O2的化学方程式:2H2O2$\frac{\underline{\;二氧化锰\;}}{\;}$2H2O+O2↑.
(5)写出③与⑦反应的离子方程式2OH-+CO2=CO32-+H2O
(6)反应Cu+4HNO3(稀)═Cu(NO3)2+2NO2↑+2H2O中,用用单线桥法表示电子得失的方向和数目:
硝酸氧化剂:还原剂铜;若消耗19.2g Cu,则被还原HNO3是0.6mol,转移0.6NA个电子.
| A. | 该元素为Mn元素 | B. | 该元素最高化合价为+7 | ||
| C. | 该元素属于d区元素 | D. | 该元素原子最外层共有7个电子 |
 .
.