题目内容
 将一定质量的镁铝合金投入200mL一定浓度的盐酸中,合金完全溶解,向所得溶液中滴加浓度为5mol/L的NaOH溶液,生成的沉淀跟加入的NaOH溶液的体积关系如图.(横坐标体积单位是mL,纵坐标质量单位是g)求:
将一定质量的镁铝合金投入200mL一定浓度的盐酸中,合金完全溶解,向所得溶液中滴加浓度为5mol/L的NaOH溶液,生成的沉淀跟加入的NaOH溶液的体积关系如图.(横坐标体积单位是mL,纵坐标质量单位是g)求:(1)合金中Mg的质量;
(2)所用盐酸的物质的量浓度.
考点:有关混合物反应的计算
专题:计算题
分析:(1)由图可知,从加入40m氢氧化钠溶液开始产生沉淀,加入氢氧化钠溶液为160mL时,沉淀量最大,此时为Mg(OH)2和Al(OH)3,该阶段消耗氢氧化钠140mL,由氢氧根守恒可知3n[Al(OH)3]+2n[Mg(OH)2]=n(NaOH)=(0.16L-0.04L)×5mol/L=0.6mol;从加入氢氧化钠溶液160mL~180mL溶解氢氧化铝,该阶段发生反应Al(OH)3+NaOH=NaAlO2+2H2O,所以n[Al(OH)3]=(0.18L-0.16L)×5mol/L=0.1mol,代入上式计算n[Mg(OH)2],由元素守恒可知n(Mg)=n[Mg(OH)2],再利用m=nM计算Mg的质量;
(2)加入氢氧化钠溶液为160mL时,沉淀量最大,此时为Mg(OH)2和Al(OH)3,溶液为氯化钠溶液,根据钠元素守恒此时溶液中n(NaCl)=n(NaOH),据此计算出n(HCl),再利用c=
计算盐酸的物质的量浓度.
(2)加入氢氧化钠溶液为160mL时,沉淀量最大,此时为Mg(OH)2和Al(OH)3,溶液为氯化钠溶液,根据钠元素守恒此时溶液中n(NaCl)=n(NaOH),据此计算出n(HCl),再利用c=
| n |
| V |
解答:
解:(1)根据图象曲线变化可知,加入40m氢氧化钠溶液开始产生沉淀,加入氢氧化钠溶液为160mL时,沉淀量最大,此时为Mg(OH)2和Al(OH)3,该阶段消耗氢氧化钠140mL,由氢氧根守恒可知:3n[Al(OH)3]+2n[Mg(OH)2]=n(NaOH)=(0.16L-0.0:4L)×5mol/L=0.6mol,
从加入NaOH溶液160mL~180mL溶解氢氧化铝,该阶段发生反应:Al(OH)3+NaOH=NaAlO2+2H2O,
则:n[Al(OH)3]=(0.18L-0.16L)×5mol/L=0.1mol,
故3×0.1mol+2n[Mg(OH)2]=0.6mol,解得n[Mg(OH)2]=0.15mol,
由元素守恒可知:n(Mg)=n[Mg(OH)2]=0.15mol,
所以Mg的质量为:0.15mol×24g/mol=3.6g,
答:合金中Mg的质量为3.6g;
(2)加入氢氧化钠溶液为160mL时,沉淀量最大,此时为Mg(OH)2和Al(OH)3,溶液为NaCl溶液,
根据钠元素守恒此时溶液中:n(NaCl)=n(NaOH)=0.16L×5mol/L=0.8mol,
根据氯元素守恒n(HCl)=0.8mol,
故盐酸的物质的量浓度为
=4mol/L,
答:盐酸的物质的量浓度为4mol/L.
从加入NaOH溶液160mL~180mL溶解氢氧化铝,该阶段发生反应:Al(OH)3+NaOH=NaAlO2+2H2O,
则:n[Al(OH)3]=(0.18L-0.16L)×5mol/L=0.1mol,
故3×0.1mol+2n[Mg(OH)2]=0.6mol,解得n[Mg(OH)2]=0.15mol,
由元素守恒可知:n(Mg)=n[Mg(OH)2]=0.15mol,
所以Mg的质量为:0.15mol×24g/mol=3.6g,
答:合金中Mg的质量为3.6g;
(2)加入氢氧化钠溶液为160mL时,沉淀量最大,此时为Mg(OH)2和Al(OH)3,溶液为NaCl溶液,
根据钠元素守恒此时溶液中:n(NaCl)=n(NaOH)=0.16L×5mol/L=0.8mol,
根据氯元素守恒n(HCl)=0.8mol,
故盐酸的物质的量浓度为
| 0.8mol |
| 0.2L |
答:盐酸的物质的量浓度为4mol/L.
点评:本题考查镁铝化合物性质、混合物的计算,题目难度中等,以图象题的形式考查,增加了试题难度,分析图象各阶段的发生的反应是解题关键,再利用守恒计算.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
已知常温下BaSO4的溶解度为2.33×10-4g,类似于水的离子积,难溶盐AmBn也有离子积Ksp且Ksp=〔C(An+)〕m?〔C(Bm-)〕n,则BaSO4的Ksp约为( )
| A、2.33×10-4 |
| B、1×10-5 |
| C、1×10-10 |
| D、1×10-12 |

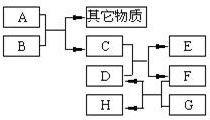 已知B为黑色粉末,用D、E、G作焰色反应,隔蓝色钴玻璃观察,焰色均呈紫色,F为深红棕色液体,H能使淀粉变蓝,它们之间的相互转化关系如图所示.
已知B为黑色粉末,用D、E、G作焰色反应,隔蓝色钴玻璃观察,焰色均呈紫色,F为深红棕色液体,H能使淀粉变蓝,它们之间的相互转化关系如图所示.