题目内容
4.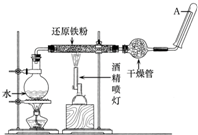 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应.应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气反应的实验”.
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应.应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气反应的实验”.请回答该实验中的问题.
(1)写出该反应的化学方程式3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.
(2)实验前必须对整套装置进行的操作是检验装置的气密性.
(3)圆底烧瓶中盛装的是水,该装置受热后的主要作用是为(硬质玻璃管内Fe与水蒸气的反应)实验提供(持续不断的)水蒸气.
(4)试管中收集到的气体是H2,如果要在A处玻璃管口处点燃该气体,则必须对该气体进行验纯.
分析 (1)Fe与水蒸气可发生反应生成四氧化三铁和氢气;
(2)该反应有气体参加和生成,装置不能漏气,且氢气不纯加热可能发生爆炸;
(3)由图可知,加热圆底烧瓶,提供水蒸气;
(4)A试管中收集到可燃性气体氢气,氢气不纯加热可能发生爆炸.
解答 解:(1)该反应的化学方程式为3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2,故答案为:3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;
(2)实验前必须对整套装置进行的操作是检验装置的气密性,故答案为:检验装置的气密性;
(3)圆底烧瓶中盛装的是水,该装置受热后的主要作用是为(硬质玻璃管内Fe与水蒸气的反应)实验提供(持续不断的)水蒸气,
故答案为:为(硬质玻璃管内Fe与水蒸气的反应)实验提供(持续不断的)水蒸气;
(4)试管中收集到的气体是H2,如果要在A处玻璃管口处点燃该气体,则必须对该气体进行验纯,故答案为:H2;验纯.
点评 本题考查物质的性质实验,为高频考点,把握物质的性质、发生的反应及实验技能等为解答的关键,侧重分析与实验能力的考查,注意氢气的性质,题目难度不大.

练习册系列答案
相关题目
16.下列物质的性质与实际应用对应关系错误的是( )
| 选项 | 物质的性质 | 实际应用 |
| A | 二氧化锰具有强氧化性 | 用作H2O2分解的氧化剂 |
| B | 液氨汽化时要吸收大量的热 | 用作制冷剂 |
| C | Al2O3熔点高 | 用作耐高温材料 |
| D | 肥皂水显碱性 | 用作蚊虫叮咬处的清洗剂 |
| A. | A | B. | B | C. | C | D. | D |
16.某校高一某化学小组欲探如下实验,想请你帮助他们完成以下实验报告:
实验目的:探究铁及其化合物的氧化性和还原性;实验所用试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、碘化钾、淀粉溶液;实验记录:
实验结论:Fe只有还原性;Fe3+只有氧化性;Fe2+既有氧化性,又有还原性.
实验目的:探究铁及其化合物的氧化性和还原性;实验所用试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、碘化钾、淀粉溶液;实验记录:
| 序号 | 实验内容 | 实验现象 | 离子方程式 | 实验结论 |
| ① | 在FeCl2溶液中滴入适量氯水 | 溶液由浅绿色变为黄色 | 2Fe2++Cl2=2Fe3++2Cl- | Fe2+具有还原性 |
| ② | 在FeCl3溶液中加入足量铁粉 | 溶液由黄色变为浅绿色 | Fe+2Fe3+=3Fe2+ | Fe3+具有氧化性 |
| ③ | 在FeCl3溶液中滴入适量KI溶液和淀粉溶液 | 溶液最终变为蓝色 | 2Fe3++2I-═2Fe2++I2 | Fe3+具有氧化性 |
13. 根据表中的信息判断下列说法错误的是( )
根据表中的信息判断下列说法错误的是( )
 根据表中的信息判断下列说法错误的是( )
根据表中的信息判断下列说法错误的是( )| 物质 | 总键能/(kJ•mol-1) | 燃烧热/(kJ•mol-1) |
| 金刚石 | a | 395.4 |
| 石墨 | b | 393.5 |
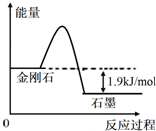
| A. | 由表中信息可得如右图所示的图象 | |
| B. | 由表中信息知C(石墨,s)=C(金刚石,s)△H=+1.9kJ/mol | |
| C. | 由表中信息可推知a<b | |
| D. | 表示石墨燃烧热的热化学方程式为C(石墨,s)+1/2O2(g)═CO(g)△H=-393.5kJ/mol |
14.某学生的实验报告所列出的下列数据中合理的是( )
| A. | 用10 mL量筒量取7.13 mL盐酸 | |
| B. | 用广泛pH试纸测得某溶液的pH为2.3 | |
| C. | 用25ml酸式滴定管量取21.70 mLKMnO4溶液 | |
| D. | 用托盘天平称量25.20 g NaCl |
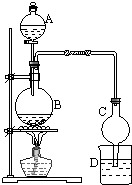 (1)某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中盛有浓硫酸,B中盛有乙醇、乙酸,D中盛有饱和碳酸钠溶液.
(1)某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中盛有浓硫酸,B中盛有乙醇、乙酸,D中盛有饱和碳酸钠溶液.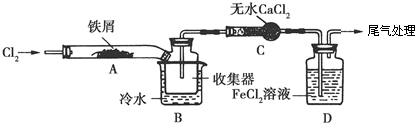
 .FeCl3是共价化合物(填“离子”或“共价”).
.FeCl3是共价化合物(填“离子”或“共价”).