题目内容
13.在氨水与NH4HCO3混合溶液中滴入FeCl2溶液,不可能发生反应的离子方程式是( )| A. | Fe2++2NH3•H2O═Fe(OH)2↓+2NH4+ | |
| B. | Fe2++NH3•H2O+HCO3-═FeCO3↓+NH4++H20 | |
| C. | Fe2++2HCO3-═Fe(OH)2↓+2CO2↑ | |
| D. | 2Fe2++HCO3-+3NH3•H2O═Fe2(OH)2CO3↓+3NH4++H2O |
分析 少量氯化亚铁,先与氨水反应生成沉淀,然后再与HCO3-反应,若氨水与NH4HCO3等物质的量反应生成碳酸根离子,还可能氨水过量较多,以此来解答.
解答 解:A.滴入少量FeCl2溶液,先与氨水反应,离子反应为Fe2++2NH3•H2O═Fe(OH)2↓+2NH4+,故A正确;
B.若氨水先与NH4HCO3反应,再滴入FeCl2溶液,发生离子反应为Fe2++NH3•H2O+HCO3-═FeCO3↓+NH4++H20,故B正确;
C.不可能Fe2+先与HCO3-反应,故C错误;
D.氨水过量时,可能发生2Fe2++HCO3-+3NH3•H2O═Fe2(OH)2CO3↓+3NH4++H2O,故D正确;
故选C.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应的离子共存考查,注意离子反应中保留化学式的物质、电荷守恒及反应的先后顺序,题目难度不大.

练习册系列答案
相关题目
16.下列说法不正确的是( )
| A. | 植物的秸秆、枝叶、杂草和人畜粪便等生物质在沼气池中经发酵可生成沼气 | |
| B. | Al(OH)3、Fe(OH)3等胶体具有很强的吸附能力,可用于净水 | |
| C. | 鸡蛋清中加入浓食盐水析出沉淀、75%乙醇溶液进行消毒、福尔马林用于浸制生物标本,其中蛋白质都发生了变性 | |
| D. | 塑料袋、废纸、旧橡胶制品等属于有机物,可以回收利用 |
1.(1)石灰工业对工农业生产意义重大,在制石灰的重要工业反应中包含着下列化学平衡:CaCO3(s)?CaO(s)+CO2(g)△H=+178.32kJ/mol现在800℃时,将CO2(g)、CaCO3(s)和CaO(s)按下列A~E不同的投料方式,放入一个10L的密闭容器中,经过足够长时间且维持温度不变,容器中CaCO3(s)的质量增加的有
A、减少的有C、D、E;体系处于化学平衡状态的有B(均填序号).(已知800℃时,该反应平衡常数K=0.003.)
(2)在岩洞、钟乳石的形成过程中包含下列反应:
CaCO3(s)+H2O(l)+CO2(g)?Ca2+(aq)+2HCO3-(aq)△H=-321.7kJ/mol
用一个不含c (Ca2+)、c (HCO3-)的表达式表示Ca (HCO3)2 溶液中的c (OH-)与其它粒子浓度间的关系:c (OH-)=c(H+)+c(H2CO3)-c(CO32-).
(3)为除去锅炉水垢中含有的CaSO4,可先用某溶液处理,使之转化为疏松、易溶于酸的物质,该转化的离子方程式是CaSO4(s)+CO32- (aq)?CaCO3(s )+SO42- (aq).
A、减少的有C、D、E;体系处于化学平衡状态的有B(均填序号).(已知800℃时,该反应平衡常数K=0.003.)
| 序号 | CaCO3/mol | CaO/mol | CO2/mol |
| A | 0.02 | 0.02 | 0.05 |
| B | 0.02 | 0.02 | 0.03 |
| C | 0.02 | 0.02 | 0.01 |
| D | 0.02 | 0 | 0.05 |
| E | 0.02 | 0.02 | 0 |
CaCO3(s)+H2O(l)+CO2(g)?Ca2+(aq)+2HCO3-(aq)△H=-321.7kJ/mol
用一个不含c (Ca2+)、c (HCO3-)的表达式表示Ca (HCO3)2 溶液中的c (OH-)与其它粒子浓度间的关系:c (OH-)=c(H+)+c(H2CO3)-c(CO32-).
(3)为除去锅炉水垢中含有的CaSO4,可先用某溶液处理,使之转化为疏松、易溶于酸的物质,该转化的离子方程式是CaSO4(s)+CO32- (aq)?CaCO3(s )+SO42- (aq).
3.下列各组反应(表中物质均为反应物),反应刚开始时,放出H2的速率最大的是( )
| 金属(粉末状)/mol | 酸的浓度及体积 | 反应温度 | |||
| A | Mg | 0.1 | 6mol/L盐酸 | 10mL | 30℃ |
| B | Mg | 0.1 | 3mol/L盐酸 | 10mL | 60℃ |
| C | Fe | 0.1 | 3mol/L盐酸 | 10mL | 60℃ |
| D | Mg | 0.1 | 6mol/L盐酸 | 10mL | 60℃ |
| A. | A | B. | B | C. | C | D. | D |
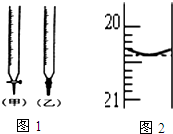 某校化学兴趣小组采用酸碱中和滴定法用0.1000mol/LNaOH溶液滴定待测盐酸溶液,试回答下面的问题:
某校化学兴趣小组采用酸碱中和滴定法用0.1000mol/LNaOH溶液滴定待测盐酸溶液,试回答下面的问题:

