题目内容
11.镍铬(Ni-Cd)可充电电池的电解质溶液为KOH溶液,它的充、放电反应按下式进行:Cd+2NiOOH+2H2O$?_{充电}^{放电}$Cd(OH)2+2Ni(OH)2;已知Ni(OH)2、Cd(OH)2和NiOOH都不溶于KOH溶液.则下列有关电极反应式或说法正确的是( )| A. | 放电时负极:Cd-2e-═Cd2+ | |
| B. | 放电时正极:2NiOOH+2e-+2H2O═2Ni(OH)2+2OH- | |
| C. | 充电时阳极:2Ni(OH)2-2e-+4H+═2Ni3++4H2O | |
| D. | 充电时含Cd的电极应与电源的正极相连 |
分析 当该电池放电时为原电池,负极上铬失电子发生氧化反应,正极上NiOOH得电子发生还原反应;当该电池充电时为电解池,阳极上Ni(OH)2失电子发生氧化反应,阴极上Cd(OH)2得电子发生还原反应,据此分析解答.
解答 解:A.放电时负极上发生的电极反应式为:Cd-2e-+2OH-=Cd(OH)2,故A错误;
B.放电时正极上发生的电极反应式为:2NiOOH+2e-+2H2O═2Ni(OH)2+2OH-,故B正确;
C.充电时阳极上发生的电极反应式为:2Ni(OH)2+2OH--2e-→2NiOOH+2H2O,故C错误;
D.充电时阴极上发生的电极反应式为:Cd(OH)2+2e-═Cd+2OH-,所以含Cd的电极应与电源的负极相连,故D错误;
故选B.
点评 本题考查电极反应式的书写,明确电极上得失电子及反应物质是解本题关键,电极反应式的书写是学习难点,要注意结合电解质溶液的酸碱性书写,难度中等.

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
19.某种氢氧燃料电池的电解质溶液为KOH溶液.下列有关该电池的叙述不正确的是( )
| A. | 正极反应式为:O2+2H2O+4e-═4OH- | |
| B. | 工作一段时间后,电解质溶液中KOH的物质的量不变 | |
| C. | 该燃料电池的总反应式为:2H2+O2═2H2O | |
| D. | 该电池工作时每消耗1molO2,有2mol电子转移 |
6.下列有关NO2的说法正确的是( )
| A. | NO2可由N2与O2反应直接制备 | |
| B. | NO2有毒,但因其易溶于水且与水反应,因此不属于大气污染物 | |
| C. | NO2既有氧化性也有还原性 | |
| D. | NO2为红棕色气体,因此将NO2通入水中,溶液显红棕色 |
3.由氧气与氢气反应生成1摩尔液态水放出285.75KJ热量,下列热化学方程式书写正确的是( )
| A. | 2H2+O2=2H2O+285.75KJ | B. | 2H2(g)+O2 (g)=2H2O(l)+571.5KJ | ||
| C. | H2(g)+O2(g)=H2O(g)+285.75KJ | D. | H2 (g)+O2(g)=H2O(l)-285.75KJ |
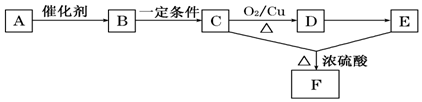

 某化学兴趣小组为探究铜与浓硫酸的反应以及SO2的性质,用右图所示装置进行有关实验.请回答下列问题:
某化学兴趣小组为探究铜与浓硫酸的反应以及SO2的性质,用右图所示装置进行有关实验.请回答下列问题: