题目内容
17.下列各组变化中,前者小于后者的是( )①CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1;
CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H2
②2H2(g)+O2(g)═2H2O(l)△H1;
H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H2
③t℃时,在一定条件下,将1mol SO2和1mol O2分别置于恒容和恒压的两个密闭容器中,达到平衡状态时反应放出的热量
④CaCO3(s)═CaO(s)+CO2(g)△H1
CaO(s)+H2O(l)═Ca(OH)2(s)△H2.
| A. | ①② | B. | ②④ | C. | ②③④ | D. | ③④ |
分析 ①甲烷燃烧生成液体水放热大于甲烷反应生成气体水;焓变包含负号比较;
②氢气和氧气反应相同条件下焓变与系数成正比;
③恒容容器中反应进行过程中压强减小,恒压容器中反应过程中压强比恒容容器中大反应物转化率大;
④碳酸钙吸热,氧化钙和水反应放热;
解答 解:①甲烷燃烧生成液体水放热大于甲烷反应生成气体水,又放热焓变为负值,所以△H1<△H2,故正确;
②2H2(g)+O2(g)═2H2O(l)△H1;H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H2,氢气的燃烧是放热的,所以焓变是负值,系数加倍,焓变数值也加倍,所以△H1=2△H2<0,所以△H1<△H2,故正确;
③在一定条件下,将1 mol SO2和1 mol O2分别置于恒容和恒压的两个密闭容器中,恒压密闭容器相当于在恒容的基础上正向移动了,所以恒P下,达到平衡状态时放出的热量更多,达到平衡状态时放出的热量分别为Q1、Q2,Q1<Q2,故正确;
④碳酸钙吸热,则焓变为正,氧化钙和水反应放热,则焓变为负,所以△H1>△H2
综上所述:①②③符合;
故选A.
点评 本题考查了反应焓变的比较,反应过程分析,反应生成物质状态的判断,物质状态不同反应热量变化不同,量不同反应热量变化不同,题目难度中等.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案
相关题目
7.下列气体不能用排空气法收集的是( )
| A. | CH4 | B. | NH3 | C. | NO2 | D. | NO |
5.已知正己烷的球棍模型为  .某有机物a的分子式和正己烷相同,且主链上有4个碳原子,则下列关于a的观点正确的是( )
.某有机物a的分子式和正己烷相同,且主链上有4个碳原子,则下列关于a的观点正确的是( )
 .某有机物a的分子式和正己烷相同,且主链上有4个碳原子,则下列关于a的观点正确的是( )
.某有机物a的分子式和正己烷相同,且主链上有4个碳原子,则下列关于a的观点正确的是( )| A. | a分子中可能有三个甲基 | |
| B. | a的分子式为C6H18 | |
| C. | a的一氯代物可能有三种 | |
| D. | 在光照条件下,a能与溴水发生取代反应 |
12.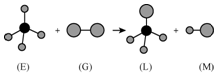 已知正四面体形分子E的直线型分子G反应,生成四面体形分子L和直线型分子M.组成E分子中的元素的原子序数都小于10,组成G分子的元素为第三周期的元素.如图,则下列判断中正确的是( )
已知正四面体形分子E的直线型分子G反应,生成四面体形分子L和直线型分子M.组成E分子中的元素的原子序数都小于10,组成G分子的元素为第三周期的元素.如图,则下列判断中正确的是( )
 已知正四面体形分子E的直线型分子G反应,生成四面体形分子L和直线型分子M.组成E分子中的元素的原子序数都小于10,组成G分子的元素为第三周期的元素.如图,则下列判断中正确的是( )
已知正四面体形分子E的直线型分子G反应,生成四面体形分子L和直线型分子M.组成E分子中的元素的原子序数都小于10,组成G分子的元素为第三周期的元素.如图,则下列判断中正确的是( )| A. | 常温常压下,L是一种液态有机物 | B. | E是一种含有非极性键的分子 | ||
| C. | 干燥的G能漂白有色物质 | D. | 上述反应的类型是取 代反应 |
2.下列关于元素性质的有关叙述中不正确的是( )
| A. | S、Cl、O、F的原子半径依次减小 | |
| B. | Na、Mg、Al、Si的失电子能力依次增强 | |
| C. | C、N、O、F的气态氢化物的稳定性依次增强 | |
| D. | Si、P、S、Cl的最高价含氧酸的酸性依次增强 |
9.下列有关叙述正确的是( )
| A. | 据悉中国在建的第二艘航母中使用了素有“现代工业的骨骼”之称的碳纤维,碳纤维是一种新型的有机高分子材料 | |
| B. | 离子交换膜在工业上应用广泛,如氯碱工业使用阴离子交换膜 | |
| C. | 获得2015年诺贝尔生理学、医学奖屠呦呦女士用乙醚从黄花蒿中提取出青蒿素,该技术应用了萃取原理 | |
| D. | 酸碱指示剂变色、煤的液化、蛋白质的颜色反应、海水提取溴、焰色反应都涉及化学变化 |
11.镍铬(Ni-Cd)可充电电池的电解质溶液为KOH溶液,它的充、放电反应按下式进行:Cd+2NiOOH+2H2O$?_{充电}^{放电}$Cd(OH)2+2Ni(OH)2;已知Ni(OH)2、Cd(OH)2和NiOOH都不溶于KOH溶液.则下列有关电极反应式或说法正确的是( )
| A. | 放电时负极:Cd-2e-═Cd2+ | |
| B. | 放电时正极:2NiOOH+2e-+2H2O═2Ni(OH)2+2OH- | |
| C. | 充电时阳极:2Ni(OH)2-2e-+4H+═2Ni3++4H2O | |
| D. | 充电时含Cd的电极应与电源的正极相连 |
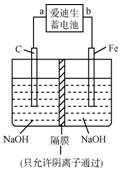 铁和铁的化合物在工业生产和日常生活中都有广泛的用途.请回答下列问题:
铁和铁的化合物在工业生产和日常生活中都有广泛的用途.请回答下列问题: