题目内容
将0.2mol?L-1的偏铝酸钠溶液和0.4mol?L-1的盐酸等体积混合,混合液中离子浓度由大到小的顺序是( )
| A、[Cl-]>[Al3+]>[Na+]>[H+]>[OH-] |
| B、[Cl-]>[Na+]>[Al3+]>[H+]>[OH-] |
| C、[Cl-]>[Al3+]>[Na+]>[OH-]>[H+] |
| D、[Na+]>[Cl-]>[Al3+]>[OH-]=[H+] |
考点:离子浓度大小的比较
专题:电离平衡与溶液的pH专题
分析:偏铝酸钠与盐酸反应的化学方程式为:NaAlO2+HCl+H2O=NaCl+Al(OH)3↓、Al(OH)3↓+3HCl=AlCl3+3H2O,设溶液体积都为1L,偏铝酸钠的物质的量为0.2mol、氯化氢的物质的量为0.4mol,0.2mol偏铝酸钠消耗0.2mol氯化氢生成0.2mol氢氧化铝沉淀,剩余的0.2molHCl会继续与氢氧化铝反应生成氯化铝,溶解的氢氧化铝的物质的量为:0.2mol×
=
mol≈0.067mol,反应后的溶液为氯化钠、氯化铝溶液,铝离子水解溶液显示酸性,据此判断溶液中各离子浓度大小.
| 1 |
| 3 |
| 1 |
| 15 |
解答:
解:设两溶液体积都是1L,则偏铝酸钠的物质的量为0.2mol、氯化氢的物质的量为0.4mol,0.2mol偏铝酸钠通过反应NaAlO2+HCl+H2O=NaCl+Al(OH)3↓消耗0.2mol氯化氢生成0.2mol氢氧化铝沉淀和0.2mol氯化钠;
剩余的0.2molHCl会继续与氢氧化铝发生反应Al(OH)3↓+3HCl=AlCl3+3H2O生成氯化铝,溶解的氢氧化铝的物质的量为:0.2mol×
=
mol≈0.067mol,溶液中铝离子的物质的量为0.067mol,
反应后的溶液中,氯离子的总物质的量为0.4mol、钠离子的物质的量为0.2mol、铝离子为0.067mol,
铝离子水解溶液显示酸性,则[H+]>[OH-],
则溶液中离子浓度大小为:[Cl-]>[Na+]>[Al3+]>[H+]>[OH-],
故选B.
剩余的0.2molHCl会继续与氢氧化铝发生反应Al(OH)3↓+3HCl=AlCl3+3H2O生成氯化铝,溶解的氢氧化铝的物质的量为:0.2mol×
| 1 |
| 3 |
| 1 |
| 15 |
反应后的溶液中,氯离子的总物质的量为0.4mol、钠离子的物质的量为0.2mol、铝离子为0.067mol,
铝离子水解溶液显示酸性,则[H+]>[OH-],
则溶液中离子浓度大小为:[Cl-]>[Na+]>[Al3+]>[H+]>[OH-],
故选B.
点评:本题考查了溶液中离子浓度大小比较,题目都能中等,正确判断发生的反应及反应物中离子的物质的量为解答关键,试题侧重考查学生的分析、理解能力及化学计算能力.

练习册系列答案
相关题目
在Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O反应中( )
| A、参加反应的硝酸和作氧化剂的硝酸质量比为2:1 |
| B、硝酸都用作氧化剂 |
| C、每个硝酸分子得到2个电子 |
| D、硝酸铜是氧化产物 |
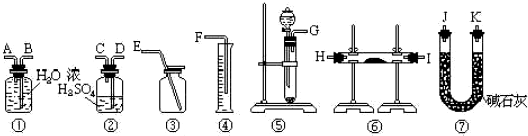
下列叙述错误的是( )
| A | B | C | D | ||||
 |  |  |  | ||||
| 闪电时会发生反应: N2+O2
| 利用丁达尔效应证明烧杯中的分散系是胶体 | 蔗糖中加入浓硫酸搅拌后变黑,因为浓硫酸有吸水性 | 加热时熔化的铝不滴落,证明Al2O3的熔点比Al高 |
| A、A | B、B | C、C | D、D |
TK时,向2.0 L恒容密闭容器中充入1.0 mol COCl2,反应COCl2(g)?Cl2(g)+CO(g),经过一段时间后达
到平衡.反应过程中测定的部分数据见下表:
下列说法正确的是 ( )
到平衡.反应过程中测定的部分数据见下表:
| t/s | 0 | 2 | 4 | 6 | 8 |
| n(Cl2)/mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
| A、保持其他条件不变,升高温度,平衡时c(Cl2)=0.22 mol?L-1,则反应的△H<0 |
| B、若在2 L恒容绝热(与外界没有热量交换)密闭容器进行该反应,化学平衡常数不变 |
| C、保持其他条件不变,起始向容器中充入1.2 molCOCl2、0.60 molCl2和0.60 molCO,反应达到平衡前的速率:v(正)<v(逆) |
| D、保持其他条件不变,起始向容器中充入1.0 molCl2和0.8 molCO,达到平衡时,Cl2的转化率小于60% |
| E、2s内,该反应的平均速率为v(COCl2)=0.175mol?L-1?s-1 |
杨老师在课堂上出示两瓶失去标签的Na2CO3和NaHCO3无色饱和溶液,希望班里同学提出简便的鉴别方法,该班同学踊跃提出看法,其中合理的是( )
| A、取同量的溶液于两支试管中,各滴入酚酞试液,红色较深的是Na2CO3 |
| B、取同量的溶液于两支试管中,加热,有气泡产生的是NaHCO3 |
| C、取同量的溶液于两支试管中,逐滴加入稀盐酸,开始就有气体放出的是NaHCO3 |
| D、取同量的溶液于两支试管中,滴加Ba(OH)2溶液,生成白色沉淀的是Na2CO3 |
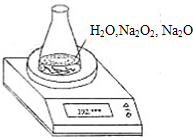 测某种含有少量氧化钠的过氧化钠试样的质量分数.
测某种含有少量氧化钠的过氧化钠试样的质量分数.