题目内容
13.下列分子中,所有原子的最外层均为8电子结构的是( )| A. | BeCl2 | B. | H2S | C. | NCl3 | D. | BF3 |
分析 根据判断的技巧:原子的最外层电子数+化合价绝对值=8,则该原子的最外层为8电子结构.
解答 解:A、铍原子最外层为4电子结构,而不是8电子结构,故A错误;
B、氢原子最外层为2电子结构,而不是8电子结构,故B错误;
C、氮原子和氯原子的最外层电子数+化合价绝对值为8,则原子的最外层均为8电子结构,故C正确;
D、BF3中,B元素化合价+其最外层电子数=3+3=6,不满足8电子结构,故D错误.
故选C.
点评 本题是对学生原子结构知识的考查,注意规律性的知识在解决选择题中的作用和地位.

练习册系列答案
相关题目
2.被称为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在另一边镀二氧化锰.在纸内是离子“流过”水和氧化锌组成的电解液.电池总反应Zn+2MnO2+H2O=ZnO+2MnO(OH),下列说法正确的是( )
| A. | 该电池的电流方向是由锌到二氧化猛 | |
| B. | 该电池反应中MnO2起催化作用 | |
| C. | 当0.1molZn完全溶解时,流经电解液的电子个数为1.204×1023 | |
| D. | 电池正极反应为2MnO2+e-+2H2O=2MnO(OH)+2OH- |
1. 在3支试管中分别放有:①1mL乙酸乙酯和3mL水 ②1mL四氯化碳和3mL水 ③1mL乙酸和3mL水.图中三支试管从左到右的排列顺序为( )
在3支试管中分别放有:①1mL乙酸乙酯和3mL水 ②1mL四氯化碳和3mL水 ③1mL乙酸和3mL水.图中三支试管从左到右的排列顺序为( )
 在3支试管中分别放有:①1mL乙酸乙酯和3mL水 ②1mL四氯化碳和3mL水 ③1mL乙酸和3mL水.图中三支试管从左到右的排列顺序为( )
在3支试管中分别放有:①1mL乙酸乙酯和3mL水 ②1mL四氯化碳和3mL水 ③1mL乙酸和3mL水.图中三支试管从左到右的排列顺序为( )| A. | ①②③ | B. | ①③② | C. | ②①③ | D. | ②③① |
2.已知A、B为短周期元素,它们的原子最外层电子数相同,且A的原子半径小于B,若m为正整数,则下列说法正确的是( )
| A. | 若HAOm是强酸,则HBOm也一定为强酸 | |
| B. | 若B为非金属元素,则A可能为金属元素,若B为金属元素,则A可能为非金属元素 | |
| C. | 常温下,若B的简单氢化物是气体,则A的简单氢化物可能是液体 | |
| D. | 若B(OH)m是强碱,则A(OH)m也是强碱 |
3.下列叙述中正确的是( )
| A. | NH3、CO、CO2都是极性分子 | |
| B. | CH4、CCl4都是含有极性键的极性分子 | |
| C. | 因为非羟基氧原子数目逐渐减少,所以酸性HClO4>H2SO4>H3PO4>HClO | |
| D. | CS2、H2O、C2H2都是直线形分子 |
 .
.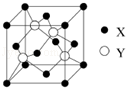 元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p 轨道上有4个电子.元素Z 的原子最外层电子数是其内层的3倍.
元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p 轨道上有4个电子.元素Z 的原子最外层电子数是其内层的3倍.