题目内容
3.下列有关物质用途的说法中,正确的是( )| A. | 小苏打常用于配制波尔多液 | B. | 氮气、氨和干冰常用作制冷剂 | ||
| C. | Fe3O4常用作红色油漆和涂料 | D. | Na2O常用作呼吸面具中氧气的来源 |
分析 A.硫酸铜、碱石灰能用于配制波尔多液;
B.液态氮气、氨气汽化时,干冰升华时吸收大量的热;
C.Fe2O3为红棕色固体;
D.过氧化钠与水、二氧化碳反应生成碳酸钠和氧气.
解答 解:A.硫酸铜、碱石灰能用于配制波尔多液,故A错误;
B.液态氮气、氨气汽化时,干冰升华时吸收大量的热,常用作制冷剂,故B正确;
C.Fe2O3为红棕色固体,常用作红色油漆和涂料,故B错误;
D.过氧化钠与水、二氧化碳反应生成碳酸钠和氧气,常用作供氧剂,氧化钠与水、二氧化碳反应不生成氧气,故D错误;
故选:B.
点评 本题考查了物质的用途,性质决定用途,明确相关物质的性质是解题关键,题目难度不大,注意对相关知识的积累.

练习册系列答案
相关题目
13.下列化学用语表述正确的是( )
| A. | 二氧化硅的分子式:SiO2 | B. | 次氯酸的电子式: | ||
| C. | Cl─的结构示意图: | D. | 四氯化碳的比例模型: |
14. 阿昔洛韦[化学名称:9-(2-羟乙氧甲基)鸟嘌呤]是抗非典型肺炎(SARS)的指定药物之一,其结构如图所示,有关阿昔洛韦的结构及性质的叙述中正确的是( )
阿昔洛韦[化学名称:9-(2-羟乙氧甲基)鸟嘌呤]是抗非典型肺炎(SARS)的指定药物之一,其结构如图所示,有关阿昔洛韦的结构及性质的叙述中正确的是( )
①分子中最多有12个原子在同一平面内;
②属于芳香族化合物;
③是一种易溶于水的醇;
④可以被氧化;⑤可以水解;
⑥可以燃烧;
⑦1mol阿昔洛韦在催化剂作用下,最多可与5molH2发生加成反应;
⑧分子式是C8H13N5O3.
 阿昔洛韦[化学名称:9-(2-羟乙氧甲基)鸟嘌呤]是抗非典型肺炎(SARS)的指定药物之一,其结构如图所示,有关阿昔洛韦的结构及性质的叙述中正确的是( )
阿昔洛韦[化学名称:9-(2-羟乙氧甲基)鸟嘌呤]是抗非典型肺炎(SARS)的指定药物之一,其结构如图所示,有关阿昔洛韦的结构及性质的叙述中正确的是( )①分子中最多有12个原子在同一平面内;
②属于芳香族化合物;
③是一种易溶于水的醇;
④可以被氧化;⑤可以水解;
⑥可以燃烧;
⑦1mol阿昔洛韦在催化剂作用下,最多可与5molH2发生加成反应;
⑧分子式是C8H13N5O3.
| A. | ①②③④⑥⑧ | B. | ②④⑤⑥ | C. | ③④⑥⑧ | D. | ④⑥⑧ |
11.含有非极性键和离子键的晶体是( )
| A. | N2 | B. | Na2O2 | C. | 金刚石 | D. | NH4Cl |
18.下列有关电解质溶液中的粒子浓度关系正确的是( )
| A. | 常温下,pH=6的NaHSO3溶液中:c(SO32-)-c(H2SO3)=9.9×10-7mol•L-1 | |
| B. | 0.1mol•L-1的NH4Cl溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| C. | 0.1mol•L-1pH=4的NaHC2O4溶液:c(H2C2O4)>c(C2O42-) | |
| D. | 向1.0L0.1mol•L-1的醋酸钠溶液中加入1.0L0.1mol•L-1盐酸:c(Na+)>c(CH3COO-)>c(H+) |
8.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温下,1L0.1mol/L的Na2CO3溶液中含有CO32-和HCO3-离子数之和为0.1NA | |
| B. | 标准状况下,11.2L丙烷中含有的极性共价键数目为4NA | |
| C. | 向Fel2溶液中通入适量Cl2,当有1molFe2+被氧化时,共转移的电子数目为NA | |
| D. | 标准状况下,22.4LCl2与足量NaOH溶液反应,转移的电子数为2NA |
5.下列对一些氢化物的沸点的比较中,错误的是( )
| A. | H2O>H2Te>H2Se>H2S | B. | HF>HI>HBr>HCl | ||
| C. | SbH3>NH3>AsH3>PH3 | D. | H2O>NH3>HF>CH4 |
2.关于如图中各装置的叙述正确的是( )
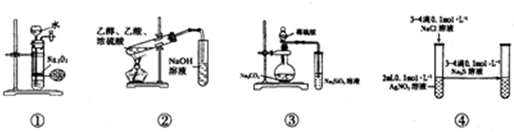

| A. | 装置①可制备少量氧气 | |
| B. | 装置②可用于实验室制取和收集乙酸乙酯 | |
| C. | 装置③的实验可推断硫、碳、硅三种元素的非金属强弱 | |
| D. | 装置④能验证AgCl沉淀可转化为溶解度更小的Ag2S沉淀 |
 )是一种名贵的香料,又是合成VE、VA、紫罗兰酮、胡萝卜素等的中间体.合成芳樟醇的一种方法如下:
)是一种名贵的香料,又是合成VE、VA、紫罗兰酮、胡萝卜素等的中间体.合成芳樟醇的一种方法如下: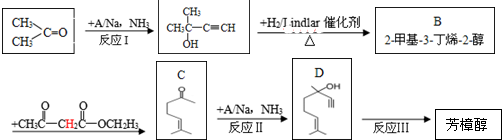
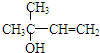 ,C分子中的官能团名称为羰基、碳碳双键,已知反应I和反应Ⅱ的原子利用率100%,则A的结构简式为HC≡CH.
,C分子中的官能团名称为羰基、碳碳双键,已知反应I和反应Ⅱ的原子利用率100%,则A的结构简式为HC≡CH.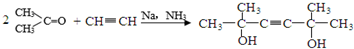 .
. ,写出柠檬醛的另一种同分异构体的结构简式(不改变分子中原子的连接方式)
,写出柠檬醛的另一种同分异构体的结构简式(不改变分子中原子的连接方式)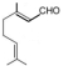 ;芳樟醇在H+作用下也可异构化为香叶醇(
;芳樟醇在H+作用下也可异构化为香叶醇(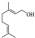 ).下列有关柠檬醛的下列说法正确的是BCD
).下列有关柠檬醛的下列说法正确的是BCD