题目内容
13.下列电子转移的表示正确的是( )| A. | 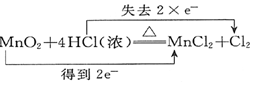 ↑+2H2O ↑+2H2O | B. | 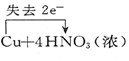 (浓)═Cu(NO3)2+2NO2↑+2H2O (浓)═Cu(NO3)2+2NO2↑+2H2O | ||
| C. | 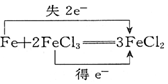 | D. | 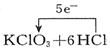 ═KCl+3Cl2↑+3H2O ═KCl+3Cl2↑+3H2O |
分析 A、二氧化锰中锰由+4价变成+2价,得到2mol电子;
B、单线桥不要标电子的得失;
C、2mol的氯化铁得到2mol的电子;
D、氯酸钾中氯得电子;
解答 解:A、二氧化锰中锰由+4价变成+2价,得到2mol电子,盐酸中只有部分氯失电子,故A正确;
B、单线桥不要标电子的得失,箭头的方向就是电子的流向,故B错误;
C、2mol的氯化铁得到2mol的电子,而不是1mol的电子,故C错误;
D、氯酸钾中氯得电子,而不是氧得电子,故D错误;
故选A.
点评 本题考查了氧化还原反应,侧重于氧化还原反应的实质和电子移转数目的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.化学平衡常数(K)、电离常数(Ka、Kb)、水的离子积(Kw)、水解常数(Kh)、溶度积常数(Ksp)等是表示、判断物质性质的重要常数,下列说法正确的是( )
| A. | 化学平衡常数的大小与温度、浓度、压强有关,与催化剂无关 | |
| B. | 降低温度时,弱酸和弱碱的电离常数(Ka、Kb)、水的离子积(Kw)均增大 | |
| C. | 向稀NaOH溶液中加入等体积等浓度的氯化镁和氯化铁混合溶液时,先产生红褐色沉淀,说明Ksp[Mg(OH)2]>Ksp[Fe(OH)3] | |
| D. | 室温下,Kh(CH3COONa)<Kh(NaCN),则等物质的量浓度时,CH3COOH的酸性比HCN弱 |
4.设NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下NA个SO3的体积为22.4 L | |
| B. | 1 mol Fe与足量的HCl反应,转移的电子数为3NA | |
| C. | 3 mol单质Fe完全转变为Fe3O4,失去8NA个电子 | |
| D. | 标准状况下,22.4 L的CCl4中含有的CCl4分子数为NA |
1.下列化合物中,既能发生消去反应,又能发生水解反应的是( )
| A. | 三氯甲烷 | B. | 2-丙醇 | C. | 2-氯丙烷 | D. | 乙酸乙酯 |
18.在给定条件下,下列选项中所示的物质间转化均能一步实现的是( )
| A. | NH3$\stackrel{O_{2}}{→}$NO2 $\stackrel{H_{2}O}{→}$HNO3 | B. | SiO2$\stackrel{HCl}{→}$SiCl4$\stackrel{H_{2}/高温}{→}$Si | ||
| C. | Al2O3$\stackrel{NaOH(aq)}{→}$NaAlO2$\stackrel{CO_{2}}{→}$Al(OH)3 | D. | Na$\stackrel{O_{2}}{→}$ Na2O2$\stackrel{CO_{2}}{→}$Na2CO3 |
5. 在25℃下,稀释HA、HB两种酸溶液,溶液pH变化的曲线如图所示,其中V1表示稀释前酸的体积,V2表示稀释后溶液的体积.下列说法正确的是( )
在25℃下,稀释HA、HB两种酸溶液,溶液pH变化的曲线如图所示,其中V1表示稀释前酸的体积,V2表示稀释后溶液的体积.下列说法正确的是( )
 在25℃下,稀释HA、HB两种酸溶液,溶液pH变化的曲线如图所示,其中V1表示稀释前酸的体积,V2表示稀释后溶液的体积.下列说法正确的是( )
在25℃下,稀释HA、HB两种酸溶液,溶液pH变化的曲线如图所示,其中V1表示稀释前酸的体积,V2表示稀释后溶液的体积.下列说法正确的是( )| A. | lg$\frac{{V}_{2}}{{V}_{1}}$=6时,HA溶液的pH=8 | |
| B. | pH相同时,c(HA)>c(HB) | |
| C. | 曲线上a、b两点 $\frac{[{B}^{-}]}{[HB][O{H}^{-}]}$ 一定不相等 | |
| D. | 25℃时,NaA溶液的pH一定小于NaB溶液 |
2.(1)刘安《淮南万毕术》中“曾青得铁则化为铜”是古代湿法炼铜的真实写照.除去CuSO4溶液中少量的Fe2+,可以按照下面的流程进行:
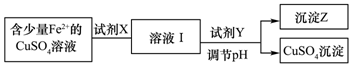
已知:Fe2+、Cu2+、Fe3+三种离子开始沉淀和完全沉淀时溶液pH值如表:
①下列物质中适合作为试剂X的是A
A.H2O2 B.KMnO4C.HNO3 D.Cl2
②加入的Y及调节的pH范围是A
A.Cu(OH)2 3.7~4.3 B.CuO 3.7~6.4
C. NaOH 3.7~4.2 D.NH3•H2O 3.7~4.0
(2)已知常温下,KspCu(OH)2]=2×10-20,通过上述流程得到的CuSO4溶液中,c(Cu2+)=0.02mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH大于5.

已知:Fe2+、Cu2+、Fe3+三种离子开始沉淀和完全沉淀时溶液pH值如表:
| 金属 离子 | pH | |
| 开始沉淀 | 完全沉淀 | |
| Fe2+ | 7.6 | 9.6 |
| Cu2+ | 4.4 | 6.4 |
| Fe3+ | 2.7 | 3.7 |
A.H2O2 B.KMnO4C.HNO3 D.Cl2
②加入的Y及调节的pH范围是A
A.Cu(OH)2 3.7~4.3 B.CuO 3.7~6.4
C. NaOH 3.7~4.2 D.NH3•H2O 3.7~4.0
(2)已知常温下,KspCu(OH)2]=2×10-20,通过上述流程得到的CuSO4溶液中,c(Cu2+)=0.02mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH大于5.
16.设NA为阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 1mol FeI2与足量氯气反应时转移的电子数为2NA | |
| B. | 常温下,56g铁片投入足量浓H2SO4中生成NA个SO2分子 | |
| C. | 1molCl2参加的氧化还原反应,反应过程中转移电子数都是2NA | |
| D. | 常温常压下,92gNO2和N2O4混合气体含有的原子数为6NA |
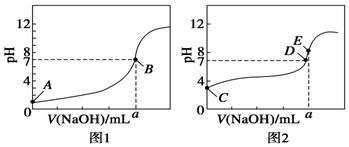 常温下,用0.100 0mol•L-1 NaOH溶液分别滴定20.00mL 0.100 0mol•L-1 HCl溶液和20.00mL 0.100 0mol•L-1 CH3COOH溶液,得到两条滴定曲线,如图所示.
常温下,用0.100 0mol•L-1 NaOH溶液分别滴定20.00mL 0.100 0mol•L-1 HCl溶液和20.00mL 0.100 0mol•L-1 CH3COOH溶液,得到两条滴定曲线,如图所示.