题目内容
17.化学与人类生活、生产息息相关,下列说法错误的是( )| A. | CuSO4具有氧化性,因此用其制成的波尔多液可用作杀菌剂 | |
| B. | 回收的地沟油可以用来制造肥皂、提取甘油或生产生物柴油 | |
| C. | 绿色化学的核心是应用化学原理从源头上减少和消除工业生产对环境的污染 | |
| D. | 纤雏素属于多糖,但不是人类的营养物质 |
分析 A.硫酸铜使蛋白质变性与氧化性无关;
B.地沟油属于油脂;
C.从源头上减少和消除工业污染,为绿色化学的核心;
D.纤维素在人体内不能消化.
解答 解:A.硫酸铜为重金属盐,使蛋白质变性与氧化性无关,故A错误;
B.地沟油属于油脂,可用于制造肥皂、提取甘油,可用于生产生物柴油,故B正确;
C.从源头上减少和消除工业污染,为绿色化学的核心,故C正确;
D.人体不含纤维素酶,纤维素在人体内不能消化,故D正确.
故选A.
点评 本题考查了化学知识在生活实际的应用,为高考常见题型,熟悉物质的组成、性质、环境保护等即可解答,题目有利于培养学生良好的科学素养,提高学习的积极性,难度不大.

练习册系列答案
相关题目
7.298K时,向50mL溶有0.1molCl2的氯水中滴加2mol•L-1的NaOH溶液,溶液pH随所加NaOH溶液体积变化的图象如下.下列说法正确的是( )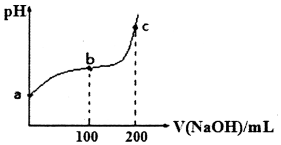

| A. | b~c段,随着NaOH溶液的滴入,$\frac{c(HClO)}{c(Cl{O}^{-})}$逐渐增大 | |
| B. | 若a点pH=4,且c(Cl-)=100c(ClO-),则Ka(HClO)=$\frac{1{0}^{-4}}{101}$ | |
| C. | b点对应的溶液可用pH试纸测定其pH | |
| D. | c点对应的溶液中:c(Na+)>c(OH-)>c(C1-)>c(C1O-)>c(H+) |
8.由下列事实得出的结论正确的是( )
| 事 实 | 结 论 | |
| A | HClO与H2SO3反应生成H2SO4和HCl | 非金属性:Cl>S |
| B | N2比白磷稳定得多 | 非金属性:N<P |
| C | 在约800℃时,金属钠可从熔融的KCl中置换出K | 金属性:Na>K |
| D | 工业上电解Na3AlF6和Al2O3的熔融混合物得到Al | 金属活动性:Na>Al |
| A. | A | B. | B | C. | C | D. | D |
5.下列有关化学实验的操作或说法中,正确的是( )
| A. | 用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液中一定不含K+ | |
| B. | 分液漏斗和容量瓶在使用前都要检漏 | |
| C. | 向某溶液中加人稀盐酸,产生的气体能使澄清石灰水变浑浊,该溶液一定是碳酸盐溶液 | |
| D. | 0.84g铁和50.00 mL 1.00 mol/L的稀硝酸反应,反应后溶液中一定只有Fe3+ |
12.X、Y、Z、W是原子序数依次增大的四种短周期元素,p、q、r、s是上述四种元素形成的二元化合物,其中r是一种中学常见的两性氧化物,s是一种强酸,r与s的水溶液反应生成P与q.下列说法错误的是( )
| A. | 简单离子半径:W>Y>Z | B. | 气态氢化物的沸点:Y>W | ||
| C. | Y与W可以形成多种二元化合物 | D. | p、q与r的化学键类型完全相同 |
2.下列有关电解质溶液说法正确的是( )
| A. | HCN溶液加水稀释,电离度保持不变,$\frac{c({F}^{-})}{c(HF)}$增大 | |
| B. | 向氨水中加入NH4Cl固体,溶液中$\frac{c(N{H}_{3}•{H}_{2}O)•c({H}^{+})}{c(N{{H}_{4}}^{+})}$增大 | |
| C. | NH4HCO3溶液呈碱性,由此可知Kb(NH3•H2O)>Ka1(H2CO3) | |
| D. | AgCl在饱和NaCl溶液中的溶解度及Ksp都比在纯水中的小 |
3.NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1.0 L 1.0 mol•L-1 的NaAlO2水溶液中含有的氧原子数为2NA | |
| B. | 25℃时,10L pH=13的Ba(OH)2溶液中含有的OH-数为2NA | |
| C. | 常温常压下,11g D218O中所含中子数为6NA | |
| D. | 某无水乙醇与足量金属钠反应生成5.6L H2,则该乙醇分子中共价键总数为4NA |