题目内容
8.由下列事实得出的结论正确的是( )| 事 实 | 结 论 | |
| A | HClO与H2SO3反应生成H2SO4和HCl | 非金属性:Cl>S |
| B | N2比白磷稳定得多 | 非金属性:N<P |
| C | 在约800℃时,金属钠可从熔融的KCl中置换出K | 金属性:Na>K |
| D | 工业上电解Na3AlF6和Al2O3的熔融混合物得到Al | 金属活动性:Na>Al |
| A. | A | B. | B | C. | C | D. | D |
分析 A.次氯酸不是最高价含氧酸,且二者发生氧化还原反应,无法据此判断非金属性;
B.N2比白磷稳定得多,与N≡N有关;
C.金属钠可从熔融的KCl中置换出K,K为气态,从平衡体系中逸出,平衡正向移动;
D.Al为活泼金属,混合物中铝离子得到电子.
解答 解:A.次氯酸具有强氧化性,HClO与H2SO3反应生成H2SO4和HCl,该反应为强酸制弱酸,且HClO不是最高价含氧酸,无法据此比较Cl、S的非金属性,故A错误;
B.N2比白磷稳定得多,与N≡N有关,而非金属性N>P,故B错误;
C.金属钠可从熔融的KCl中置换出K,K为气态,从平衡体系中逸出,平衡正向移动,反应才能发生,而金属性K>Na,故C错误;
D.Al为活泼金属,电解法冶炼金属时,混合物中铝离子得到电子,钠离子没有得到电子,可知金属性Na>Al,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握发生的反应、非金属性和金属性比较方法为解答的关键,侧重分析与评价能力的考查,注意比较非金属性的角度,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.设NA为阿伏加德罗常数的数值.下列有关叙述不正确的是( )
| A. | 44g乙醛中所含的氧原子数为NA | |
| B. | 足量的铜与40mL10mol/L硝酸反应,生成气体的分子数为0.2NA | |
| C. | 14g乙稀中所含的C-H键数目为2NA | |
| D. | 0.1molNH3中所含的电子数为NA |
16.下列关于有机物的说法,正确的是( )
| A. | 己知异丙苯的纺构简式为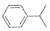 ,则异丙苯中碳原子可能处于同一平面 ,则异丙苯中碳原子可能处于同一平面 | |
| B. | 分子式为C4H9Cl的有机物共有4种同分异构体 | |
| C. | 乙酸和溴乙烷在一定条件下均可发生加成反应 | |
| D. | 油脂和蛋白质都属于高分子化合物 |
3.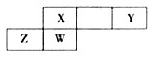 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中X元素形成的化合物种类最多.下列说法错误的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中X元素形成的化合物种类最多.下列说法错误的是( )
 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中X元素形成的化合物种类最多.下列说法错误的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中X元素形成的化合物种类最多.下列说法错误的是( )| A. | 原子半径:Z>W>X>Y | |
| B. | 工业上用Y和Z组成的化合物冶炼Z的单质 | |
| C. | X、Y形成的化合物一定为酸性氧化物 | |
| D. | W的单质和氧化物均可与NaOH溶液反应 |
13.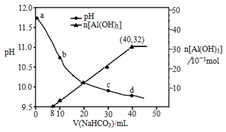 用过量烧碱溶液处理某铝土矿(含Al2O3、Fe2O3),过滤后得到滤液用NaHCO3溶液处理,测得溶液pH和Al(OH)3生成的量随加入NaHCO3溶液体积变化的曲线如下:下列有关说法不正确的是( )
用过量烧碱溶液处理某铝土矿(含Al2O3、Fe2O3),过滤后得到滤液用NaHCO3溶液处理,测得溶液pH和Al(OH)3生成的量随加入NaHCO3溶液体积变化的曲线如下:下列有关说法不正确的是( )
 用过量烧碱溶液处理某铝土矿(含Al2O3、Fe2O3),过滤后得到滤液用NaHCO3溶液处理,测得溶液pH和Al(OH)3生成的量随加入NaHCO3溶液体积变化的曲线如下:下列有关说法不正确的是( )
用过量烧碱溶液处理某铝土矿(含Al2O3、Fe2O3),过滤后得到滤液用NaHCO3溶液处理,测得溶液pH和Al(OH)3生成的量随加入NaHCO3溶液体积变化的曲线如下:下列有关说法不正确的是( )| A. | V(NaHCO3)<8mL时,发生的反应为HCO3-+OH-═CO32-+H2O | |
| B. | b点与c点溶液所含微粒种类相同 | |
| C. | NaHCO3溶液的物质的量浓度为0.8 mol•L-1 | |
| D. | 生成沉淀的离子方程式为:HCO3-+AlO2-+H2O═Al(OH)3↓+CO32- |
20.设NA表示阿伏伽德罗常数的值.下列有关叙述正确的是( )
| A. | 50g 98%的硫酸中含有氧原子数目为2NA | |
| B. | 1L0.1 mol•L-1氨水中含有OH-的数目为0.1NA | |
| C. | 标准状况下,22.4L由CCl4和CH2O组成的混合物中含碳原子数目为NA | |
| D. | 常温常压下,足量的Al与1 molCl2共热充分反应后,转移电子数目为2NA |
17.化学与人类生活、生产息息相关,下列说法错误的是( )
| A. | CuSO4具有氧化性,因此用其制成的波尔多液可用作杀菌剂 | |
| B. | 回收的地沟油可以用来制造肥皂、提取甘油或生产生物柴油 | |
| C. | 绿色化学的核心是应用化学原理从源头上减少和消除工业生产对环境的污染 | |
| D. | 纤雏素属于多糖,但不是人类的营养物质 |
12.下列与有机物结构、性质相关的叙述错误的是( )
| A. | 乙醛和丙烯醛( )不是同系物,但它们与H2充分反应后的产物是同系物 )不是同系物,但它们与H2充分反应后的产物是同系物 | |
| B. | 一分子β-月桂烯(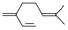 )与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 )与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有3种 | |
| C. | 用甘氨酸(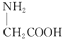 )和丙氨酸( )和丙氨酸(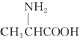 )缩合最多可形成4种二肽 )缩合最多可形成4种二肽 | |
| D. | 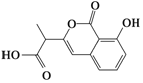 和 和 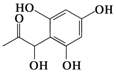 都既能与NaOH溶液反应,能与溴水反应,但与两种试剂反应的原因都不完全相同 都既能与NaOH溶液反应,能与溴水反应,但与两种试剂反应的原因都不完全相同 |