题目内容
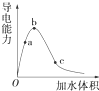 一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示.
一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示.(1)O点导电能力为0的理由
(2)a、b、c三点溶液的c(H+)由小到大的顺序是
(3)a、b、c三点醋酸的电离程度最大的是
(4)要使c点c(CH3COO-)增大,c(H+)减少,可采取的措施是(至少写出四种方法)
①
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:(1)溶液的导电性与离子浓度有关,离子浓度越大,导电性越强;
(2)导电能力越强,离子浓度越大,氢离子浓度越大,pH越小;
(3)溶液越稀,越促进醋酸电离,则溶液中氢离子的物质的量越大;
(4)要使醋酸根离子浓度增大,可以采用加热、加入含有醋酸根离子的物质、加入和氢离子反应的物质.
(2)导电能力越强,离子浓度越大,氢离子浓度越大,pH越小;
(3)溶液越稀,越促进醋酸电离,则溶液中氢离子的物质的量越大;
(4)要使醋酸根离子浓度增大,可以采用加热、加入含有醋酸根离子的物质、加入和氢离子反应的物质.
解答:
解:(1)溶液的导电性与离子浓度有关,离子浓度越大,导电性越强,冰醋酸中没有自由移动的离子,所以冰醋酸不导电,故答案为:无自由移动的离子;
(2)导电能力越强,离子浓度越大,氢离子浓度越大,pH越小,则a、b、c三点溶液的pH为b<a<c,故答案为:b<a<c;
(3)溶液越稀,越促进醋酸电离,则溶液中氢离子的物质的量越大,所以氢离子物质的量最大的是c,故答案为:c;
(4)要使醋酸根离子浓度增大,c(H+)减少,可以采用消耗氢离子的方法使电离平衡向正方向移动、故可以加入氢氧化钠固体;碳酸钠固体;镁等金属;或者增加醋酸根浓度使电离向逆方向移动,故可加醋酸钠固体等,故答案为:氢氧化钠固体;碳酸钠固体;镁等金属;醋酸钠固体.
(2)导电能力越强,离子浓度越大,氢离子浓度越大,pH越小,则a、b、c三点溶液的pH为b<a<c,故答案为:b<a<c;
(3)溶液越稀,越促进醋酸电离,则溶液中氢离子的物质的量越大,所以氢离子物质的量最大的是c,故答案为:c;
(4)要使醋酸根离子浓度增大,c(H+)减少,可以采用消耗氢离子的方法使电离平衡向正方向移动、故可以加入氢氧化钠固体;碳酸钠固体;镁等金属;或者增加醋酸根浓度使电离向逆方向移动,故可加醋酸钠固体等,故答案为:氢氧化钠固体;碳酸钠固体;镁等金属;醋酸钠固体.
点评:本题考查电解质的电离,题目难度中等,易错选项是D,加水稀释醋酸,能促进醋酸电离,但溶液中醋酸根离子增大的量远远小于水体积增大的量,所以醋酸根离子浓度减小,为易错点.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
分别取40mL的0.50mol/L盐酸与40mL0.55mol/L氢氧化钠溶液进行中和热的测定.下列说法错误的是( )
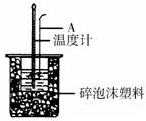

| A、稍过量的氢氧化钠是确保盐酸完全反应 |
| B、仪器A的名称是环形玻璃搅拌棒 |
| C、在实验过程中,如果不把温度计上的酸用水冲洗干净直接测量NaOH溶液的温度,则测得的△H偏大 |
| D、用Ba(OH)2和硫酸代替盐酸和氢氧化钠溶液,结果也是正确的 |
哈伯因发明了由氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖.现向一密闭容器中充入1mol N2和3mol H2,在一定条件下使该反应发生:N2+3H2
2NH3,下列有关说法正确的是( )
| 高温、高压 |
| 催化剂 |
| A、达到化学平衡时,N2将完全转化为NH3 |
| B、达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等 |
| C、达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化 |
| D、达到化学平衡时,正反应和逆反应的速率都为零 |
工业制硫酸中的一步重要反应是SO2在400~500℃下的催化氧化:2SO2+O2
2SO3,这是一个正反应放热的可逆反应.如果反应在密闭容器中进行,下述有关说法中错误的是( )
| V2O5 |
| △ |
| A、使用催化剂是为了加快反应速率,提高生产效率 |
| B、在上述条件下,SO2不可能100%地转化为SO3 |
| C、为了提高SO2的转化率,应适当提高O2的浓度 |
| D、达到平衡时,SO2的浓度与SO3的浓度相等 |
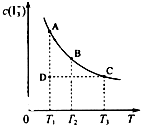 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq),某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法不正确的是( )
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq),某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态).下列说法不正确的是( )| A、反应 I2(aq)+I-(aq)?I3-(aq) 的△H<0 |
| B、若反应进行到状态D时,一定有v正>v逆 |
| C、状态A与状态B相比,状态A的c(I2)大 |
| D、若温度为T1,T2反应的平衡常数分别为K1、K2,则K1>K2 |
下列说法错误的是( )
| A、由电能转化为化学能的装置叫电解池 |
| B、在电解池中跟直流电源的正极相连的电极是电解池的阳极 |
| C、在电解池中通电时,电子从电解池的阴极流出,并沿导线流回电源的负极 |
| D、电解池中阴极发生还原反应,阳极发生氧化反应 |
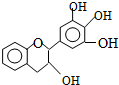 “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )| A、分子中只有2个手性碳原子 |
| B、1molEGC与4molNaOH恰好完全反应 |
| C、可发生氧化反应和取代反应,不能发生加成反应 |
| D、遇FeCl3溶液会发生显色反应 |
