题目内容
18.下列反应类型与苯和浓硝酸反应类型相同的是( )| A. | 甲烷和氯气混合并光照 | B. | 乙醇和酸性高锰酸钾溶液的反应 | ||
| C. | 乙烯生成聚乙烯 | D. | 苯和氢气反应生成环己烷 |
分析 苯与浓硝酸在浓硫酸做催化剂的作用下加热反应生成硝基苯,该反应属于取代反应,然后根据有机反应的概念及各选项的反应类型进行判断.
解答 解:苯与浓硝酸生成硝基苯的反应属于取代反应,
A.甲烷与氯气在光照条件下发生的反应为取代反应,故A正确;
B.乙醇和酸性高锰酸钾溶液发生氧化还原反应,故B错误;
C.乙烯发生加聚反应生成聚乙烯,故C错误;
D.苯和氢气发生加成反应生成环己烷,故D错误.
故选A.
点评 本题考查了有机反应类型及判断,为高频考点,题目难度不大,注意掌握常见有机物的概念、类型及判断方法,明确取代反应与消去反应、加成反应的区别,把握常见有机物的性质以及反应类型的判断.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
6.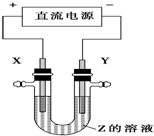 利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )
利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )
 利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )
利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )| A. | 氯碱工业中,X、Y均为石墨,X附近能得到氢氧化钠 | |
| B. | 铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4 | |
| C. | 在铁片上镀铜时,Y是纯铜 | |
| D. | 外加电流的阴极保护法中,Y是待保护金属 |
3.在150℃时,某气态混合烃和过量O2在一密闭容器中完全反应,测知反应前后压强没有变化,则该混合烃可能是( )
| A. | CH4和C2H4 | B. | CH4和C2H6 | C. | C2H4和C2H6 | D. | C3H4和C3H6 |
10.除去小苏打溶液中少量苏打的方法是( )
| A. | 加热 | B. | 加NaOH | C. | 通CO2气体 | D. | 加盐酸 |
7.六种短周期元素A、B、C、D、E、F的原子序数依次增大,其中A与E同主族,B与F同主族,E与F同周期.已知常温下单质A与E的状态不同,D的核电荷数是B的最外层电子数的2倍,单质F是一种重要的半导体材料.则下列推断中正确的是( )
| A. | A、C两种元素仅可组成化学式为CA3的化合物 | |
| B. | F与D形成的化合物性质很不活泼,不与任何酸反应 | |
| C. | 原子半径由大到小的顺序是E>F>C>D | |
| D. | 元素的非金属性由强到弱的顺序是D>C>F>B |
8.向amolNaOH的溶液中通入bmolCO2,下列说法不正确的是( )
| A. | 当a:b>2时,发生的离子反应为:2OH-+CO2═CO32-+H2O | |
| B. | 当a:b<1时,发生的离子反应为:OH-+CO2═HCO3- | |
| C. | 当2a=3b时,发生的离子反应为:2OH-+CO2═CO32-+H2O | |
| D. | 当0.5a<b<a时,溶液中HCO3-与CO32-共存 |