题目内容
8.某化学实验小组制备硫酸亚铁铵晶体并设计实验测定其组成,他们进行了以下实验:I.向FeSO4溶液中加入饱和(NH4)2SO4溶液,经过“一系列操作”后得到一种浅蓝绿色的硫酸亚铁铵晶体,这种晶体俗名“摩尔盐”,它比绿矾(FeSO4•7H2O)要稳定得多.将此摩尔盐低温烘干后,称取7.84g加热至100℃失去全部结晶水,质量变为5.68g
II.选择如图所示的部分装置连接起来,检查气密性后,将上述5.68g固体放入A装置的锥形瓶中,再向锥形瓶中加入足量NaOH浓溶液,充分吸收产生的气体并测出气体质量为0.68g.
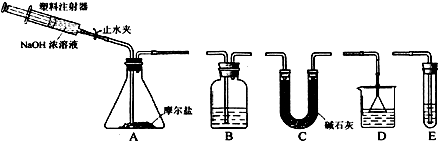
III.向A中加入适量3%的H2O2溶液,充分振荡后滤出沉淀,洗净、干燥、灼烧后,测得其质量为1.6g.
根据上述实验回答下列问题:
(1)实验I中,要检验FeSO4溶液中是否含有Fe3+常用的试剂是KSCN溶液,“一系列操作”依次为蒸发浓缩、冷却结晶和过滤.
(2)实验II中,选择的装置是A接C接D(填代号),A装置中未使用分液漏斗的理由是NaOH溶液对分液漏斗活塞、旋塞的磨口腐蚀性强.
(3)向锥形瓶中加入NaOH溶液的操作方法是打开止水夹,缓慢推压注射器活塞,吸收A中产生的气体所用试剂应是H2SO4溶液,实验小组的同学为保证A中产生的气体被完全吸收,以准确测量其质量,他们在A中反应停止后再进行的操作是用注射器向A中注入空气,使装置中的氨气全部进入吸收液.
(4)根据上述实验数据计算,7.84g摩尔盐中SO42-的质量为3.84g,摩尔盐中n(NH${\;}_{4}^{+}$):n(Fe2+):(SO${\;}_{4}^{2-}$):n(H2O)=2:1:2:6.
分析 (1)可用KSCN检验Fe3+,由溶液制备晶体,可进行蒸发浓缩、冷却结晶、过滤等操作;
(2)莫尔盐与氢氧化钠溶液反应生成氨气,可用稀硫酸吸收,注意防止倒吸,氢氧化钠具有强腐蚀性,可与二氧化硅反应;
(3)加入氢氧化钠溶液时,应先打开止水夹,缓慢推压注射器活塞,用稀硫酸吸收氨气,为保证气体完全吸收,可用注射器向A中注入空气;
(4)由题给数据可知7.84g摩尔盐中m(H2O)=7.84g-5.68g=2.16g,生成的m(NH3)=0.68g,m(Fe2O3)=1.6g,以此可确定SO42-的质量以及n(NH4+):n(Fe2+):n((SO42-):n(H2O)的比值.
解答 解:(1)可用KSCN检验Fe3+,如含Fe3+,则加入KSCN,溶液变为血红色,由溶液制备晶体,可进行蒸发浓缩、冷却结晶、过滤等操作,
故答案为:KSCN溶液;蒸发浓缩;冷却结晶;
(2)莫尔盐与氢氧化钠溶液反应生成氨气,生成氨气先用碱石灰干燥,以除去水,然后用稀硫酸在D装置内吸收氨气,以防止倒吸,氢氧化钠具有强腐蚀性,可与二氧化硅反应,则可用注射器加入氢氧化钠溶液,
故答案为:C、D; NaOH溶液对分液漏斗活塞、旋塞的磨口腐蚀性强;
(3)加入氢氧化钠溶液时,应先打开止水夹,缓慢推压注射器活塞,用稀硫酸吸收氨气,为保证气体完全吸收,可用注射器向A中注入空气,使装置中的氨气全部进入吸收液,
故答案为:打开止水夹,缓慢推压注射器活塞;H2SO4溶液;用注射器向A中注入空气,使装置中的氨气全部进入吸收液;
(4)由题给数据可知7.84g摩尔盐中m(H2O)=7.84g-5.68g=2.16g,n(H2O)=$\frac{2.16g}{18g/mol}$=0.12mol,
生成的m(NH3)=0.68g,m(Fe2O3)=1.6g,
则n(NH3)=$\frac{0.68g}{17g/mol}$=0.04mol,n(Fe2O3)=$\frac{1.6g}{160g/mol}$=0.01mol,
则m(NH4+)=0.04mol×18g/mol=0.72g,m(Fe2+)=0.02mol×56g/mol=1.12g,
则m(SO42-)=7.84g-2.16g-0.72g-1.12g=3.84g,
n(SO42-)=$\frac{3.84g}{96g/mol}$=0.04mol,
所以n(NH4+):n(Fe2+):n((SO42-):n(H2O)=0.04mol:0.02mol:0.04mol:0.12mol=2:1:2:6,
故答案为:3.84;2:1:2:6.
点评 本题考查物质的含量测定,侧重于学生的分析能力、计算能力和实验能力的考查,题目难度中等,注意把握相关实验基本方法和注意事项.

 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案| A. | Ga(OH)3酸性强于Al(OH)3 | B. | Al(OH)3酸性强于Ga(OH)3 | ||
| C. | Ga(OH)3碱性强于Al(OH)3 | D. | Al(OH)3碱性强于Ga(OH)3 |
| A. | 4 mol | B. | 3 mol | C. | 2.5mol | D. | 1.2 mol |
| A. | 2c(H+)═2c(HS-)+c(S2-)+2c(OH-)? | B. | c(H+)═c(HS-)+2c(S2-)+c(OH-) | ||
| C. | c(H+)═c(HS-)+2c(S2-)? | D. | c(H+)═2c(S2-)+c(OH-)? |
已知:
生成氢氧化物沉淀的pH
| Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀时 | 8.3 | 6.3 | 2.7 | 4.7 |
| 完全沉淀时 | 9.8 | 8.3 | 3.7 | 6.7 |
| 化学式 | FeS | CuS | MnS |
| 溶度积 | 6.3×10-18 | 1.3×10-36 | 2.5×10-13 |
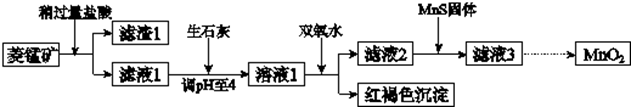
(1)滤渣1为SiO2;
(2)向溶液1中加入双氧水时,反应的离子方程式是2Fe2++H2O2+4H2O=2Fe(OH)3↓+4H+;
(3)滤液2中加入稍过量的难溶电解质MnS,以除去Cu2+,反应的离子方程式是MnS+Cu2+=Mn2++CuS;在CuS、MnS共存的悬浊液中,则$\frac{c(C{u}^{2+})}{c(M{n}^{2+})}$=5.2×10-24.
(4)将MnCl2转化为MnO2的一种方法是氧化法.其具体做法是用酸化的NaClO3溶液将MnCl2氧化,该反应的离子方程式为:5Mn2++2ClO3-+□4H2O═□Cl2↑+□5MnO2+□8H+;
(5)将MnCl2转化为MnO2的另一种方法是电解法.
①生成MnO2的电极反应式是Mn2+-2e-+2H2O=MnO2+4H+;
②若直接电解MnCl2溶液,生成MnO2的同时会产生少量Cl2,检验Cl2的操作是将润湿的淀粉碘化钾试纸置于阳极附近,若试纸变蓝则证明有Cl2生成.
| A. | 甲烷和氯气混合并光照 | B. | 乙醇和酸性高锰酸钾溶液的反应 | ||
| C. | 乙烯生成聚乙烯 | D. | 苯和氢气反应生成环己烷 |
 如图是实验室制取并探究氯气化学性质的装置图
如图是实验室制取并探究氯气化学性质的装置图 .
. ,A2C的结构式:H-O-H.
,A2C的结构式:H-O-H. .
.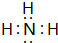 ,请用电子式表示A与C形成化合物的过程
,请用电子式表示A与C形成化合物的过程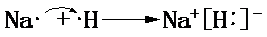 .
.