题目内容
5.某混合气体由一种气态烷烃A和一种气态烯烃B组成,在同温同压下,该混合气体的平均相对分子质量是氢气相对分子质量的12倍,取31.2g该混合气体通入足量的溴水中,溴水质量增重16.8g,通过计算回答:(1)求混合气体中气态烷烃A和气态烯烃B的分子式
(2)混合气体中A和B的物质的量之比是多少?
分析 (1)根据混合气体与氢气的相对分子质量关系计算出混合气体的平均分子量,根据计算结果及烯烃、烷烃的相对分子质量可判断越大含有甲烷;然后根据n=$\frac{m}{M}$计算出31.2g混合气体的物质的量,溴水增重的为烯烃的质量,据此可知甲烷的质量,然后根据n=$\frac{m}{M}$计算出混合气体中甲烷的物质的量,从而可知烯烃的摩尔质量,再结合烯烃的通式确定其分子式;
(2)设出烷烃和烯烃的物质的量,利用平均摩尔质量列式计算出二者物质的量之比.
解答 解:(1)在同温同压下,该混合气体的平均相对分子质量是氢气相对分子质量的12倍,则该混合气体的平均相对分子质量为:12×2=24,烷烃和烯烃中相对分子质量小于24的只有甲烷,所以混合气体中一定含有CH4;
31.2g该混合气体的物质的量为:$\frac{31.2g}{24g/mol}$=1.3mol,溴水增重的16.8g为烯烃的质量,则该混合气体中含有甲烷的物质的量为:$\frac{31.2g-16.8g}{16g/mol}$=0.9mol,
该烯烃的摩尔质量为:$\frac{16.8g}{1.3mol-0.9mol}$=42g/mol,该烯烃为丙烯,分子式为C3H6,
答:混合气体中烷烃A为CH4,烯烃B为C3H6;
(2)设甲烷的物质的量为x,丙烯的物质的量为y,则:$\frac{16x+42y}{x+y}$=24,整理可得x:y=9:4,则甲烷与丙烯的物质的量之比为9:4,
答:混合气体中甲烷与丙烯的物质的量之比为9:4.
点评 本题考查了混合物反应的计算,题目难度中等,明确烷烃、烯烃的组成及性质为解答关键,注意掌握平均值法在化学计算中的应用,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
3.用括号内的试剂可除去各组物质中的少量杂质,使物质得到提纯的是( )
| A. | 乙醇中的水(Na) | B. | 乙酸乙酯中的乙醇(乙酸) | ||
| C. | 乙酸乙酯中的乙酸(饱和Na2CO3溶液) | D. | 乙酸中的苯酚(NaOH溶液) |
13.在相同条件下,H2和CO的混合气体VL,完全燃烧时需O2的体积是( )
| A. | 2VL | B. | VL | C. | 0.5VL | D. | 无法计算 |
14.下列物质属于弱电解质的是( )
| A. | CO2 | B. | NH3•H2O | C. | HCl | D. | AgNO3 |
15.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 饱和氯水中 Br-、NO3-、Na+、SO32- | |
| B. | 由水电离出的C(H+)=1×10 -12 mol•L-1的溶液:K+、Ba2+、HCO3-、Cl- | |
| C. | 0.1 mol•L-1FeCl3溶液:K+、NH4+、NO3-、SO42- | |
| D. | c(H+)/c(OH-)=1×10 -12的溶液:Ca2+、Fe3+、ClO-、NO3- |
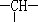 和一个-Cl,它的可能的结构有几种( )
和一个-Cl,它的可能的结构有几种( )