题目内容
3.用括号内的试剂可除去各组物质中的少量杂质,使物质得到提纯的是( )| A. | 乙醇中的水(Na) | B. | 乙酸乙酯中的乙醇(乙酸) | ||
| C. | 乙酸乙酯中的乙酸(饱和Na2CO3溶液) | D. | 乙酸中的苯酚(NaOH溶液) |
分析 A.乙醇、水均与Na反应;
B.乙醇、乙醇、乙酸乙酯互溶;
C.乙酸与饱和碳酸钠反应后,与乙酸乙酯分层;
D.二者均与NaOH溶液反应.
解答 解:A.乙醇、水均与Na反应,则Na不能除杂,故A不选;
B.乙醇、乙醇、乙酸乙酯互溶,则不能除杂,故B不选;
C.乙酸与饱和碳酸钠反应后,与乙酸乙酯分层,然后分液可分离,故C选;
D.二者均与NaOH溶液反应,不能除杂,故D不选;
故选C.
点评 本题考查混合物的分离提纯,为高频考点,把握有机物的性质、性质差异、混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意有机物性质的应用,题目难度不大.

练习册系列答案
相关题目
14.下表是元素周期表中短周期元素的一部分,表中所列字母分别代表一种元素.
(1)写出H的元素符号:Si
(2)画出E的离子结构示意图
(3)化合物AK的电子式是 .
.
(4)在一定条件下,A与D可形成一种极易溶于水的气态化合物,其化学式为NH3;该物质溶于水后的溶液呈碱性(填“酸”“碱”或“中”).
(5)K的氢化物比J的氢化物稳定,其原因是K比J得电子能力强.
(6)在这些元素的最高价氧化物对应水化物中,碱性最强的是NaOH(填化学式)
(7)F的最高价氧化物对应的水化物和K的最高价氧化物对应的水化物的反应化学方程式NaOH+HClO4═NaClO4+H2O;F的最高价氧化物对应的水化物和G的最高价氧化物对应的水化物的反应化学方程式NaOH+Al(OH)3═NaAlO2+H2O.
| A | B | ||||||
| C | D | E | |||||
| F | G | H | I | J | K |
(2)画出E的离子结构示意图

(3)化合物AK的电子式是
 .
.(4)在一定条件下,A与D可形成一种极易溶于水的气态化合物,其化学式为NH3;该物质溶于水后的溶液呈碱性(填“酸”“碱”或“中”).
(5)K的氢化物比J的氢化物稳定,其原因是K比J得电子能力强.
(6)在这些元素的最高价氧化物对应水化物中,碱性最强的是NaOH(填化学式)
(7)F的最高价氧化物对应的水化物和K的最高价氧化物对应的水化物的反应化学方程式NaOH+HClO4═NaClO4+H2O;F的最高价氧化物对应的水化物和G的最高价氧化物对应的水化物的反应化学方程式NaOH+Al(OH)3═NaAlO2+H2O.
1.某地污水含有Zn2+、Hg2+、Fe3+和Cu2+四种阳离子,甲、乙、丙三位同学设计的从该污水中回收金属铜的方案如下:
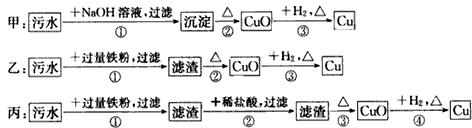
下列判断正确的是( )

下列判断正确的是( )
| A. | 三种实验方案中都能制得纯净铜 | |
| B. | 甲方案中的反应涉及置换、分解、复分解三种反应类型 | |
| C. | 乙方案中加过量铁粉只能还原其中的二种阳离子 | |
| D. | 丙方案不会产生环境污染 |
8. 二甲醚(CH3OCH3)是一种应用前景广阔的清洁燃料,以CO和H2为原料生产二甲醚主要发生以下三个反应:
二甲醚(CH3OCH3)是一种应用前景广阔的清洁燃料,以CO和H2为原料生产二甲醚主要发生以下三个反应:
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
由上述数据计算△H1=-99 kJ•mol-1;
(2)该工艺的总反应为3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)△H,该反应△H=-263 kJ•mol-1,化学平衡常数K=K12•K2•K3(用含K1、K2、K3的代数式表示);
(3)下列措施中,能提高CH3OCH3产率的有AD;
A.分离出二甲醚 B.升高温度
C.改用高效催化剂 D.增大压强
(4)工艺中反应①和反应②分别在不同的反应器中进行,无反应③发生.该工艺中反应③的发生提高了CH3OCH3的产率,原因是反应③消耗了反应②中的产物H2O,使反应②的化学平衡向正反应方向移动,从而提高CH3OCH3的产率;
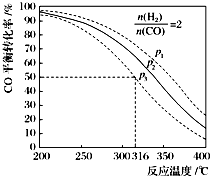
(5)以$\frac{n({H}_{2})}{n(CO)}$=2 通入1L的反应器中,一定条件下发生反应:4H2(g)+2CO(g)?CH3OCH3(g)+H2O(g)△H,其CO的平衡转化率随温度、压强变化关系如图所示.下列说法正确的是CD;
A.该反应的△H>0
B.若在p2和316℃时反应达到平衡,则CO的转化率小于50%
C.若在p3和316℃时反应达到平衡,H2的转化率等于50%
D.若在p3和316℃时,起始时$\frac{n(H2)}{n(CO)}$=3,则达平衡时CO的转化率大于50%
E.若在p1和200℃时,反应达平衡后保持温度和压强不变,再充入2mol H2和1mol CO,则平衡时二甲醚的体积分数增大
(6)某温度下,将8.0mol H2和4.0mol CO充入容积为2L的密闭容器中,发生反应:4H2(g)+2CO(g)?CH3OCH3(g)+H2O(g),反应达平衡后测得二甲醚的体积分数为25%,则该温度下反应的平衡常数K=2.25.
 二甲醚(CH3OCH3)是一种应用前景广阔的清洁燃料,以CO和H2为原料生产二甲醚主要发生以下三个反应:
二甲醚(CH3OCH3)是一种应用前景广阔的清洁燃料,以CO和H2为原料生产二甲醚主要发生以下三个反应:| 编号 | 热化学方程式 | 化学平衡常数 |
| ① | CO(g)+2H2(g)?CH3OH(g)△H1 | K1 |
| ② | 2CH3OH(g)?CH3OCH3(g)+H2O(g)△H2=-24kJ•mol-1 | K2 |
| ③ | CO(g)+H2O(g)?CO2(g)+H2(g)△H3=-41kJ•mol-1 | K3 |
(1)已知反应①中的相关的化学键键能数据如下:
| 化学键 | H-H | C-O | C=O | H-O | C-H |
| E/(kJ.mol-1) | 436 | 343 | 1076 | 465 | 413 |
(2)该工艺的总反应为3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)△H,该反应△H=-263 kJ•mol-1,化学平衡常数K=K12•K2•K3(用含K1、K2、K3的代数式表示);
(3)下列措施中,能提高CH3OCH3产率的有AD;
A.分离出二甲醚 B.升高温度
C.改用高效催化剂 D.增大压强
(4)工艺中反应①和反应②分别在不同的反应器中进行,无反应③发生.该工艺中反应③的发生提高了CH3OCH3的产率,原因是反应③消耗了反应②中的产物H2O,使反应②的化学平衡向正反应方向移动,从而提高CH3OCH3的产率;
(5)以$\frac{n({H}_{2})}{n(CO)}$=2 通入1L的反应器中,一定条件下发生反应:4H2(g)+2CO(g)?CH3OCH3(g)+H2O(g)△H,其CO的平衡转化率随温度、压强变化关系如图所示.下列说法正确的是CD;
A.该反应的△H>0
B.若在p2和316℃时反应达到平衡,则CO的转化率小于50%
C.若在p3和316℃时反应达到平衡,H2的转化率等于50%
D.若在p3和316℃时,起始时$\frac{n(H2)}{n(CO)}$=3,则达平衡时CO的转化率大于50%
E.若在p1和200℃时,反应达平衡后保持温度和压强不变,再充入2mol H2和1mol CO,则平衡时二甲醚的体积分数增大
(6)某温度下,将8.0mol H2和4.0mol CO充入容积为2L的密闭容器中,发生反应:4H2(g)+2CO(g)?CH3OCH3(g)+H2O(g),反应达平衡后测得二甲醚的体积分数为25%,则该温度下反应的平衡常数K=2.25.
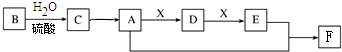
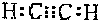 .
.