题目内容
17.实验室中需要标准状况下5.6L的CO2,现有含CaCO3 90%的石灰石与250mL足量的稀盐酸反应,该石灰石中的杂质不与盐酸反应,问:(1)需要的CO2的质量是多少克?
(2)至少需要含CaCO390%的石灰石多少克?
(3)生成CaCl2的物质的量是多少?
分析 发生反应CaCO3+2HCl=CaCl2+H2O+CO2↑,设至少需要含碳酸钙90.0%的石灰石的质量为x,则碳酸钙质量为90%x,设生成的氯化钙的物质的量y,根据方程式中定量关系计算.
解答 解:设至少需要含碳酸钙90.0%的石灰石的质量为x,生成的氯化钙的物质的量y,盐酸的物质的量为z,则
CaCO3+2HCl=CaCl2+H2O+CO2↑
100g 2mol 1mol 22.4L
90%x z y 5.6L
$\frac{100}{90%x}=\frac{1}{y}=\frac{22.4}{5.6}$
解之得:x=$\frac{100g×5.6L}{22.4L×90%}$=27.8g
y=$\frac{1mol×5.6L}{22.4L}$=0.25mol
需要的CO2的质量是$\frac{5.6}{22.4}×44$克=11克,
答:(1)需要的CO2的质量是11克;
(2)至少需要含碳酸钙90.0%的石灰石27.8g;
(3)生成的氯化钙的物质的量是0.25mol.
点评 本题考查化学方程式的有关计算,关键是理解方程式中各个物理量之间的关系,注意左右单位不一致时,应左右单位相当,上下单位一致.

练习册系列答案
相关题目
14.下表是元素周期表中短周期元素的一部分,表中所列字母分别代表一种元素.
(1)写出H的元素符号:Si
(2)画出E的离子结构示意图
(3)化合物AK的电子式是 .
.
(4)在一定条件下,A与D可形成一种极易溶于水的气态化合物,其化学式为NH3;该物质溶于水后的溶液呈碱性(填“酸”“碱”或“中”).
(5)K的氢化物比J的氢化物稳定,其原因是K比J得电子能力强.
(6)在这些元素的最高价氧化物对应水化物中,碱性最强的是NaOH(填化学式)
(7)F的最高价氧化物对应的水化物和K的最高价氧化物对应的水化物的反应化学方程式NaOH+HClO4═NaClO4+H2O;F的最高价氧化物对应的水化物和G的最高价氧化物对应的水化物的反应化学方程式NaOH+Al(OH)3═NaAlO2+H2O.
| A | B | ||||||
| C | D | E | |||||
| F | G | H | I | J | K |
(2)画出E的离子结构示意图

(3)化合物AK的电子式是
 .
.(4)在一定条件下,A与D可形成一种极易溶于水的气态化合物,其化学式为NH3;该物质溶于水后的溶液呈碱性(填“酸”“碱”或“中”).
(5)K的氢化物比J的氢化物稳定,其原因是K比J得电子能力强.
(6)在这些元素的最高价氧化物对应水化物中,碱性最强的是NaOH(填化学式)
(7)F的最高价氧化物对应的水化物和K的最高价氧化物对应的水化物的反应化学方程式NaOH+HClO4═NaClO4+H2O;F的最高价氧化物对应的水化物和G的最高价氧化物对应的水化物的反应化学方程式NaOH+Al(OH)3═NaAlO2+H2O.
8. 二甲醚(CH3OCH3)是一种应用前景广阔的清洁燃料,以CO和H2为原料生产二甲醚主要发生以下三个反应:
二甲醚(CH3OCH3)是一种应用前景广阔的清洁燃料,以CO和H2为原料生产二甲醚主要发生以下三个反应:
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
由上述数据计算△H1=-99 kJ•mol-1;
(2)该工艺的总反应为3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)△H,该反应△H=-263 kJ•mol-1,化学平衡常数K=K12•K2•K3(用含K1、K2、K3的代数式表示);
(3)下列措施中,能提高CH3OCH3产率的有AD;
A.分离出二甲醚 B.升高温度
C.改用高效催化剂 D.增大压强
(4)工艺中反应①和反应②分别在不同的反应器中进行,无反应③发生.该工艺中反应③的发生提高了CH3OCH3的产率,原因是反应③消耗了反应②中的产物H2O,使反应②的化学平衡向正反应方向移动,从而提高CH3OCH3的产率;
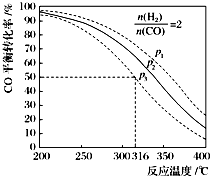
(5)以$\frac{n({H}_{2})}{n(CO)}$=2 通入1L的反应器中,一定条件下发生反应:4H2(g)+2CO(g)?CH3OCH3(g)+H2O(g)△H,其CO的平衡转化率随温度、压强变化关系如图所示.下列说法正确的是CD;
A.该反应的△H>0
B.若在p2和316℃时反应达到平衡,则CO的转化率小于50%
C.若在p3和316℃时反应达到平衡,H2的转化率等于50%
D.若在p3和316℃时,起始时$\frac{n(H2)}{n(CO)}$=3,则达平衡时CO的转化率大于50%
E.若在p1和200℃时,反应达平衡后保持温度和压强不变,再充入2mol H2和1mol CO,则平衡时二甲醚的体积分数增大
(6)某温度下,将8.0mol H2和4.0mol CO充入容积为2L的密闭容器中,发生反应:4H2(g)+2CO(g)?CH3OCH3(g)+H2O(g),反应达平衡后测得二甲醚的体积分数为25%,则该温度下反应的平衡常数K=2.25.
 二甲醚(CH3OCH3)是一种应用前景广阔的清洁燃料,以CO和H2为原料生产二甲醚主要发生以下三个反应:
二甲醚(CH3OCH3)是一种应用前景广阔的清洁燃料,以CO和H2为原料生产二甲醚主要发生以下三个反应:| 编号 | 热化学方程式 | 化学平衡常数 |
| ① | CO(g)+2H2(g)?CH3OH(g)△H1 | K1 |
| ② | 2CH3OH(g)?CH3OCH3(g)+H2O(g)△H2=-24kJ•mol-1 | K2 |
| ③ | CO(g)+H2O(g)?CO2(g)+H2(g)△H3=-41kJ•mol-1 | K3 |
(1)已知反应①中的相关的化学键键能数据如下:
| 化学键 | H-H | C-O | C=O | H-O | C-H |
| E/(kJ.mol-1) | 436 | 343 | 1076 | 465 | 413 |
(2)该工艺的总反应为3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g)△H,该反应△H=-263 kJ•mol-1,化学平衡常数K=K12•K2•K3(用含K1、K2、K3的代数式表示);
(3)下列措施中,能提高CH3OCH3产率的有AD;
A.分离出二甲醚 B.升高温度
C.改用高效催化剂 D.增大压强
(4)工艺中反应①和反应②分别在不同的反应器中进行,无反应③发生.该工艺中反应③的发生提高了CH3OCH3的产率,原因是反应③消耗了反应②中的产物H2O,使反应②的化学平衡向正反应方向移动,从而提高CH3OCH3的产率;
(5)以$\frac{n({H}_{2})}{n(CO)}$=2 通入1L的反应器中,一定条件下发生反应:4H2(g)+2CO(g)?CH3OCH3(g)+H2O(g)△H,其CO的平衡转化率随温度、压强变化关系如图所示.下列说法正确的是CD;
A.该反应的△H>0
B.若在p2和316℃时反应达到平衡,则CO的转化率小于50%
C.若在p3和316℃时反应达到平衡,H2的转化率等于50%
D.若在p3和316℃时,起始时$\frac{n(H2)}{n(CO)}$=3,则达平衡时CO的转化率大于50%
E.若在p1和200℃时,反应达平衡后保持温度和压强不变,再充入2mol H2和1mol CO,则平衡时二甲醚的体积分数增大
(6)某温度下,将8.0mol H2和4.0mol CO充入容积为2L的密闭容器中,发生反应:4H2(g)+2CO(g)?CH3OCH3(g)+H2O(g),反应达平衡后测得二甲醚的体积分数为25%,则该温度下反应的平衡常数K=2.25.
2.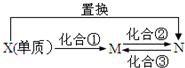 M、N为含X元素的常见化合物,它们之间有如图的转化关系.下列说法正确的是( )
M、N为含X元素的常见化合物,它们之间有如图的转化关系.下列说法正确的是( )
 M、N为含X元素的常见化合物,它们之间有如图的转化关系.下列说法正确的是( )
M、N为含X元素的常见化合物,它们之间有如图的转化关系.下列说法正确的是( )| A. | X可以是Mg或Cu元素 | |
| B. | 化合②③的反应可以是非氧化还原反应 | |
| C. | 若X为C元素,则该转化关系中X单质发生的置换反应可以是2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO | |
| D. | 若X为Fe元素,则M的H218O溶液中加入固体Na2O2的反应为:4Fe3++6H218O+6Na2O2═4Fe(OH)3↓+12Na++318O2↑ |
9.镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用.已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd+2NiOOH+2H2O$?_{充电}^{放电}$Cd(OH)2+2Ni(OH)2有关该电池的说法正确的是( )
| A. | 放电时负极得电子,质量减轻 | |
| B. | 放电时电解质溶液中的OH-向正极移动 | |
| C. | 充电时阴极附近溶液的pH减小 | |
| D. | 充电时阳极反应:Ni(OH)2-e-+OH-═NiOOH+H2O |
7.下列关于元素周期表中递变规律的说法正确的是( )
| A. | 同主族元素从上到下,单质的熔点逐渐降低 | |
| B. | 同周期主族元素离子半径从左到右依次减小 | |
| C. | HF、HCl、HBr、HI 的热稳定性依次减弱,还原性和水溶液的酸性依次增强 | |
| D. | 第三周期非金属元素含氧酸的酸性从左到右依次增强 |
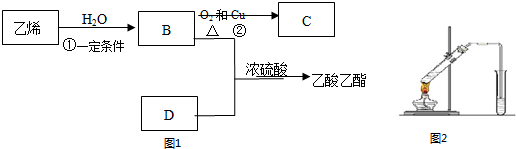
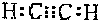 .
.