题目内容
6.水玻璃溶液敞口放置空气中会变质,主要是因为与X反应生成Y,则X和Y分别是( )| A. | CO2和H4SiO4 | B. | O2和SiO2 | C. | CO2和Na2CO3 | D. | H2和NaOH |
分析 水玻璃为硅酸钠溶液,硅酸酸性弱于碳酸,所以二氧化碳通入硅酸钠溶液反应生成原硅酸和碳酸钠,据此解答.
解答 解:水玻璃为硅酸钠溶液,硅酸酸性弱于碳酸,依据强酸制备弱酸规律,二氧化碳通入硅酸钠溶液反应生成原硅酸和碳酸钠,方程式:CO2+Na2SiO3+2H2O=H4SiO4↓+CO32-,所以X为二氧化碳,Y为H4SiO4,
故选:A.
点评 本题考查了元素化合物性质,题目难度不大,熟悉硅酸盐性质是解题关键,注意强酸制备弱酸的规律.

练习册系列答案
相关题目
1.某一溶液中含amol FeCl3和bmol CuCl2,向其中加入足量的铁粉,充分反应后,再过滤,残渣质量小于加入的铁粉质量,则a:b( )
| A. | 小于2:7 | B. | 等于2:7 | C. | 大于2:7 | D. | 无法肯定 |
18.如图,将铁棒和石墨棒插入盛有饱和NaCl溶液的U形管中,下列分析正确的是( )
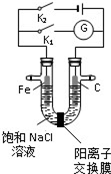

| A. | K1闭合,铁棒侧溶液会出现白色沉淀,而且沉淀最终变为红褐色 | |
| B. | K1或 K2闭合,石墨棒周围溶液 pH 均升高 | |
| C. | K2闭合,铁棒上发生的反应为 2Cl--2e-═Cl2↑ | |
| D. | K2闭合,电路中通过 0.002NA个电子时,两极共产生 0.002mol 气体 |
15.下列说法正确的是(NA表示阿伏加德罗常数的值)( )
| A. | 1 mol聚乙烯含有的原子数目为6NA | |
| B. | 标准状况下1 L己烷完全燃烧后恢复至原状态,生成气态物质分子数为$\frac{5{N}_{A}}{22.4}$ | |
| C. | 1 mol甲基含10NA个电子 | |
| D. | 2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |