题目内容
16.科学家制造出一种使用固体电解质的燃料电池,其效率更高.一个电极通入空气,另一个电极通入汽油蒸汽.其中固体电解质是掺杂了Y2O3(Y:钇)的ZrO2(Zr:锆) 固体,它在高温下能传导O2-离子.以戊烷(C5H12)代表汽油,完成下列问题:①电池反应方程式为C5H12+8O2=5CO2+6H2O;
②放电时固体电解质里的O2-离子的移动方向是向负极移动(填“正”或“负”).
分析 一个电极通入空气,另一个电极通入汽油蒸汽,则氧气在正极得到电子,C5H12在负极失去电子,阴离子向负极移动,以此来解答.
解答 解:①由信息可知,氧气在正极得到电子,C5H12在负极失去电子,电池反应为C5H12+8O2=5CO2+6H2O,故答案为:C5H12+8O2=5CO2+6H2O;
②原电池中阴离子向负极移动,则放电时固体电解质里的O2-离子的移动方向是向负极移动,故答案为:负.
点评 本题考查原电池及工作原理,为高频考点,把握原电池的工作原理、电极反应、离子移动等为解答的关键,侧重分析与应用能力的考查,注意电池反应与燃烧反应的区别,题目难度不大.

练习册系列答案
 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目
6.水玻璃溶液敞口放置空气中会变质,主要是因为与X反应生成Y,则X和Y分别是( )
| A. | CO2和H4SiO4 | B. | O2和SiO2 | C. | CO2和Na2CO3 | D. | H2和NaOH |
7.下列物质属于纯净物的是( )
①天然气 ②铝热剂 ③纯碱 ④漂白粉 ⑤胆矾 ⑥纯净的矿泉水⑦氢氧化铁胶体.
①天然气 ②铝热剂 ③纯碱 ④漂白粉 ⑤胆矾 ⑥纯净的矿泉水⑦氢氧化铁胶体.
| A. | ①③⑤⑥ | B. | ③⑤⑥ | C. | ②④⑦ | D. | ③⑤ |
11.下列离子组能够大量共存的是( )
| A. | 无色溶液中:Cu2+、K+、NO3-、Cl- | |
| B. | 使pH试纸显红色的溶液中:Fe2+、K+、NO3-、Cl- | |
| C. | 含MnO4-的溶液中:Fe3+、SO42-、NO3-、Mg2+ | |
| D. | 与铝作用生成氢气的溶液中:Mg2+、NO3-、K+、Cl- |
8.下列离子方程式书写正确的是( )
| A. | 在100ml 1mol•L-1的Fe(NO3)3的溶液中通入足量SO2:2Fe3++SO2+2H2O═2Fe2++SO42-+4H+ | |
| B. | 在100ml 2mol•L-1的FeI2的溶液中通入标况下5.6L的Cl2:4Fe2++6I-+5Cl2═4Fe3++3I2+10Cl- | |
| C. | 向NaHCO3溶液中加入过量的澄清石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- | |
| D. | AlCl3溶液中加入过量的NaOH溶液:Al3++4OH-═AlO2-+2H2O |
5.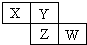 X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
 X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )| A. | X的气态氢化物能与其最高价氧化物对应的水化物反应生成盐 | |
| B. | 原子半径:X<Y | |
| C. | Z的非金属性比Y的强 | |
| D. | X与Y形成的化合物都易溶于水 |
6.下列反应一定属于放热反应的是( )
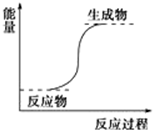

| A. | 氢氧化钡晶体和氯化铵晶体的反应 | |
| B. | 能量变化如图所示的反应 | |
| C. | 化学键断裂吸收的能量比化学键形成放出的能量少的反应 | |
| D. | 不需要加热就能发生的反应 |

