��Ŀ����
14���ȱ�����Ҫ���л�������Ʒ����Ⱦ�ϡ�ҽҩ���л��ϳɵ��м��壬��ҵ�ϳ��á���Ъ������ȡ����Ӧԭ����ʵ��װ��ͼ������װ�ö�����ȥ�����£�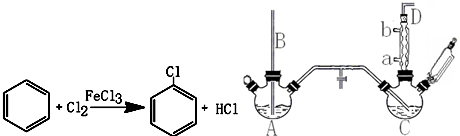
��֪���ȱ�Ϊ��ɫҺ�壬�е�132.2�森
�ش��������⣺
��1��A��Ӧ��������ʵ���ҷ���ȡ�������пղ�����B��������ƽ����ѹ������������ˮӦ��a���a����b����a��ͨ�룮
��2���Ѹ��������ͨ��װ�и��ﱽ�ķ�Ӧ��C�У������൱�ڱ���1%����м��������������ά�ַ�Ӧ�¶���40��60��Ϊ�ˣ��¶ȹ������ɶ��ȱ���
�ٶ�C���ȵķ�����c������ţ�
�ƾ��Ƽ��� b����ԡ���� c��ˮԡ����
��D���ڵ�����ɷ���HCl����������������
��3��C��Ӧ����Ӧ��ɺ�ҵ��Ҫ����ˮϴ����ϴ��ʳ�θ����������ϴ֮ǰҪˮϴ��Ŀ����ϴȥ�������ͬʱ���ټ����������Լ�ɱ���д����10%�������Ƽ�ϴʱ���ܷ����Ļ�ѧ��Ӧ����ʽ��FeCl3+3NaOH=Fe��OH��3��+3NaCl��HCl+NaOH=NaCl+H2O��д�������ɣ���
��4������װ��ͼ��A��C��Ӧ��֮�䣬��Ҫ����һ��U�ιܣ������������������������Ȼ��ƣ�
���� ��1��������B����Һ���£�װ����ѹǿ����ʱ����������ƽ����ѹ����ȡ����ԭ��ͨ������ˮ��
��2���ٷ�Ӧ��C���ȿ��Ʒ�Ӧ�¶���40-60�棬Ӧ����ˮԡ���ȣ�
�����ڱ��ӷ�����Ӧ������HCl������δ��Ӧ��������������D���ڵ�����
��3�������Ȼ������������Ʒ�Ӧ�����ɵ�HCl�����������Ʒ�Ӧ���ܽ������Ҳ����ȥ�����Ʒ�Ӧ��
��4��A��C��Ӧ��֮����Ҫ��������װ�ã��������ɵ������������������������Ȼ��Ƶȣ�
��� �⣺��1��������B����Һ���£�װ����ѹǿ����ʱ����������ƽ����ѹ����ȡ����ԭ��ͨ������ˮ��ʹ�����ܳ�������ˮ�������ȴ��������ˮ��a�����룬��b��������
�ʴ�Ϊ��ƽ����ѹ��a��
��2���ٷ�Ӧ��C���ȿ��Ʒ�Ӧ�¶���40-60�棬Ӧ����ˮԡ���ȣ�
�ʴ�Ϊ��c��
�����ڱ��ӷ�����Ӧ������HCl������δ��Ӧ��������D���������к���HCl����������������
�ʴ�Ϊ����������������
��3���ڴ����Ȼ������������Ʒ�Ӧ������HCl�����������Ʒ�Ӧ���ܽ������Ҳ����ȥ�����Ʒ�Ӧ����Ӧ����ʽΪ��FeCl3+3NaOH=Fe��OH��3��+3NaCl��HCl+NaOH=NaCl+H2O��Cl2+2NaOH=NaCl+NaClO+H2O��
�ʴ�Ϊ��FeCl3+3NaOH=Fe��OH��3��+3NaCl��HCl+NaOH=NaCl+H2O�ȣ�
��4��A��C��Ӧ��֮����Ҫ����U�ܣ��������ɵ������������������������Ȼ��Ƶȣ�
�ʴ�Ϊ�������������Ȼ��ƣ�
���� ���⿼���л����Ʊ�ʵ�鷽������Ŀ�Ѷ��еȣ��漰��װ�á�������ԭ���ķ������۵�֪ʶ����ȷʵ��Ŀ�ġ�ʵ��ԭ��Ϊ���ؼ�������������ѧ���ķ�����������ѧʵ��������

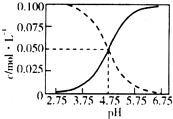 25��ʱ��c��CH3COOH��+c��CH3COO-��=0.1mol•L-1�Ĵ��ᡢ�����ƻ����Һ�У�c��CH3COOH����c��CH3COO-����pH�Ĺ�ϵ��ͼ��ʾ������������ȷ���ǣ�������
25��ʱ��c��CH3COOH��+c��CH3COO-��=0.1mol•L-1�Ĵ��ᡢ�����ƻ����Һ�У�c��CH3COOH����c��CH3COO-����pH�Ĺ�ϵ��ͼ��ʾ������������ȷ���ǣ�������| A�� | 25��ʱ��CH3COOH�ĵ��볣��K��ֵ5��10-2.75 | |
| B�� | ��pH����$\frac{c��C{H}_{3}COOH��}{c��C{H}_{3}CO{O}^{-}��}$���� | |
| C�� | pH=4����Һ�У�c��CH3COO-����c��CH3COOH����c��H+����c��OH-�� | |
| D�� | pH=5����Һ�У�c��H+��+c��Na+��+c��CH3COOH��-c��OH-��=0.1 mol•L-1 |
| Ԫ�ش��� | A | B | C | D | E |
| ԭ�Ӱ뾶/nm | 0.186 | 0.143 | 0.089 | 0.104 | 0.074 |
| ��Ҫ���ϼ� | +1 | +3 | +2 | +6��-2 | -2 |
| A�� | BԪ�ز����γɹ��ۻ����� | |
| B�� | ���Ӱ뾶��СA+��D2- | |
| C�� | A��E�γɵĻ�������ֻ���ܺ����Ӽ� | |
| D�� | B��E�Ļ����ﲻ�����ڰ�ˮ |
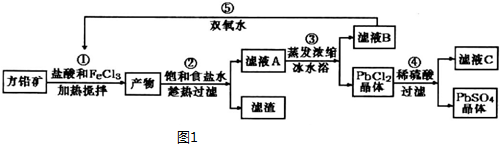
��֪����Ksp��PbSO4��=1.08��10-8��Ksp��PbCl2��=1.6��l0-5��
��PbCl2��s��+2C1-��aq��?PbCl42-��aq����H��0
��Fe3+��Pb2+������������ʽ��ʼ����ʱ��PHֵ�ֱ�Ϊ1.9��7��
��1�������м���������Կ�����Һ��pH��1.9����ҪĿ��������Fe3+��ˮ�⣮
��Ӧ�����пɹ۲쵽����ɫ��������ٶ�Ӧ�����ӷ���ʽΪ2Fe3++PbS=PbCl2+S+2Fe2+��
��2�������õ���ҺA����Ũ�������ñ�ˮԡ��Ŀ�����ñ�ˮԡʹPbCl2��s��+2Cl-��aq��?PbCl4-��H��0�����ƶ���ʹPbCl4-ת��PbCl2����������ƽ���ƶ�ԭ�����ͣ�
��3�����ж�Ӧ��Ӧ��ƽ�ⳣ������ʽ$\frac{{c}^{2}��C{l}^{-}��}{c��S{{O}_{4}}^{2-}��}$��
��4�����������п�ѭ�����õ�������FeCl3��HCl��
��5����Ǧ����Ǧ����ʹˮ�����ؽ���Ǧ�ĺ�����������������Ⱦ��ˮ��Һ��Ǧ�Ĵ�����̬��Ҫ��Pb2+��Pb��OH��+��Pb��OH��2��Pb��OH��3-��Pb��OH��42-������̬��ǦŨ�ȷ���x����ҺpH�仯�Ĺ�ϵ��ͼ2��ʾ��
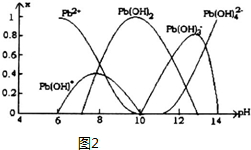
��̽��Pb2+�����ʣ���Pb2+����Һ����εμ�NaOH����Һ����ǣ������μ�NaOH��Һ�ֱ���壻pH��13ʱ����Һ�з�������Ҫ��Ӧ�����ӷ���ʽΪPb��OH��3-+HO-=Pb��OH��42-����
�ڳ�ȥ��Һ�е�Pb2+������С����һ�������Լ���ȥ��ˮ�еĺ���Ǧ�������������ӣ�ʵ������¼���£�
| ���� | Pb2+ | Ca2+ | Fe3+ | Mn2+ |
| ����ǰŨ��/��mg•L-1�� | 0.100 | 29.8 | 0.12 | 0.087 |
| ������Ũ��/��mg•L-1�� | 0.004 | 22.6 | 0.04 | 0.053 |
���������Լ���DH������Ǧ��������Ҫ�����ķ�ӦΪ��2DH��s��+Pb2+?D2Pb��s��+2H+������Ǧʱ����ʵ�pHԼΪ6��
��֪���ٽ���Һ���е���������Ҫ��H+��Co2+��Fe2+��Mn2+��Ca2+��Mg2+��Al3+�ȣ�
�ڲ���������������������ʽ����ʱ��Һ��pH���±���
| ������ | Fe��OH��3 | Fe��OH��2 | Co��OH��2 | Al��OH��3 | Mn��OH��2 |
| ��ȫ������pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
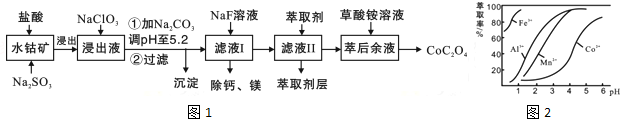
��2����ȡNaClO3���Խ�����ͨ�뵽�ȵ�Ũ����������Һ���÷�Ӧ�����ӷ���ʽΪ3Cl2+6OH-$\frac{\underline{\;\;��\;\;}}{\;}$ClO3-+5Cl-+3H2O��ʵ����Ҫ��ȡ10.65��NaClO3����Ҫ�������ɵ��ʳ��ˮ���ɣ��������Ƿ�Ӧ�����е���ʧ����ͬʱ���ɵ����������Ϊ6.72����״������
��3����ȡ���Խ������ӵ���ȡ����pH�Ĺ�ϵ��ͼ2��ʾ����Һ���м�����ȡ���������dz�ȥMn2+��ʹ����ȡ�����˵�pH��B����ѡ����ţ���
A���ӽ�2.0 B���ӽ�3.0 C���ӽ�5.0
��4�������ơ�þ���ǽ���Һ��Ca2+��Mg2+ת��ΪMgF2��CaF2��������֪Ksp��MgF2��=7.35��10-11��Ksp��CaF2��=1.05��10-10�����������NaF��������Һc��Mg2+��/c��Ca2+��=0.7��
��5����ҵ���ð�ˮ���շ����е�SO2����֪NH3•H2O�ĵ���ƽ�ⳣ��K=1.8��10-5mol•L��H2SO3�ĵ���ƽ�ⳣ��K1=1.2��10-2mol•L-4��K2=1.3��10-8mol•L-1����ͨ������Ĺ����У�
�ٵ�ǡ���γ�����ʱ����Һ������Ũ�ȵĴ�С��ϵΪc��NH4+����c��SO32-����c��OH-����c��HSO3-����c��H+����
�ڵ�ǡ���γ���ʽ��ʱ����������NaOH��Һ����Ӧ�����ӷ���ʽΪHSO3-+OH-=SO32-+H2O��
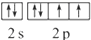 ����Ԫ�صķ�����O��
����Ԫ�صķ�����O��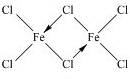 ������Ϊ�÷����Ƿ�Ϊƽ���η��ӣ�����ǡ�����
������Ϊ�÷����Ƿ�Ϊƽ���η��ӣ�����ǡ�����