题目内容
8.一定温度下1mol NH4HS固体在定容真空容器中可部分分解为硫化氢和氨气,当反应达平衡时ρ氢气×ρ硫化氢=a(Pa2),则容器中的总压为( )| A. | 2aPa | B. | 2$\sqrt{a}$Pa | C. | $\frac{2}{3}$aPa | D. | 无法确定 |
分析 发生反应为NH4HS=NH3+H2S,NH4HS分解生成等物质的量的硫化氢和氨气,NH3与H2S的分压相同,结合ρ氢气×ρ硫化氢=a(Pa2)计算.
解答 解:NH4HS=NH3+H2S,由NH4HS分解的反应方程式可知:生成等物质的量的硫化氢和氨气,则NH3与H2S的分压相同,故p硫化氢=p氨气=$\sqrt{a}$Pa所以,平衡后的总压为p硫化氢+p氨气=2$\sqrt{a}$Pa,
故选:B.
点评 本题考查了有关方程式的计算,题目难度不大,侧重于考查学生的分析能力和对题干信息的应用能力,注意把握物质的量与压强的关系.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.下列各组离子在溶液中按括号内的物质的量之比混合,得到无色、澄清溶液的是( )
| A. | Fe3+、Na+、Cl-、S2-(1:2:3:1) | B. | NH4+、Ba2+、OH-、NO3-(1:1:1:2) | ||
| C. | K+、H+、I-、AlO2-(1:1:1:1) | D. | Na+、Al3+、Cl-、OH-(4:1:4:3) |
19.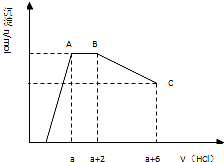 某溶液中可能含有OH-,CO32-,AlO2-,SiO32-,SO42-,K+,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示(已知::AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-)),下列结论不正确的是( )
某溶液中可能含有OH-,CO32-,AlO2-,SiO32-,SO42-,K+,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示(已知::AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-)),下列结论不正确的是( )
 某溶液中可能含有OH-,CO32-,AlO2-,SiO32-,SO42-,K+,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示(已知::AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-)),下列结论不正确的是( )
某溶液中可能含有OH-,CO32-,AlO2-,SiO32-,SO42-,K+,Na+,Fe3+,Mg2+,Al3+等离子,当向溶液中逐滴加入盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图所示(已知::AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-)),下列结论不正确的是( )| A. | 溶液中一定不存在的离子:Fe3+,Mg2+,Al3+ | |
| B. | AB段可得到能使澄清的石灰水变浑浊的气体 | |
| C. | c(CO32-):c(AlO2-)=2:3 | |
| D. | BC段发生反应的离子方程式为Al(OH)3+3H+═Al3++3H2O |
16.常温下,关于pH=10的氨水和氢氧化钠溶液,下列说法正确的是( )
| A. | n(NH3•H2O)>n(NaOH) | |
| B. | 在氢氧化钠溶液中,c(OH)=1010mol/L | |
| C. | 在氨水中,c(OH)=c(NH4)+c(H) | |
| D. | 0.1mol/L的盐酸分别与等体积的氨水和氢氧化钠溶液恰好完全反应,氨水消耗的盐酸体积少 |
13.5.6g铁粉投入到足量的100mL 2mol/L的稀硫酸中,2min时铁粉刚好溶解,下列表示这个反应的速率正确的是( )
| A. | v(H2SO4)=0.5 mol/(L•min) | B. | v(H2SO4)=1 mol/(L•min) | ||
| C. | v(H+)=0.5 mol/(L•min) | D. | v(FeSO4)=0.5 mol/(L•min) |
20.用如图所示的装置电解KBr溶液制取KBrO3,生成16.7g KBrO3时理论上转移电子的物质的量为( )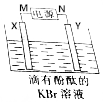

| A. | 0.1mol | B. | 0.2mol | C. | 0.4mol | D. | 0.6mol |
17.120℃时,将H2、C2H5OH、O2的混合气体通入盛有足量Na2O2的密闭容器中,用电火花不断点燃,反应完全后,体系内压强为零,则混合气体中,H2、C2H5OH、O2的物质的量之比可能是( )
| A. | 3:4:1 | B. | 3:1:2 | C. | 7:2:1 | D. | 9:3:1 |
1.化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
| A. | 氯原子的电子排布式3s23p5 | B. | Cl-的结构示意图  | ||
| C. | 氯离子的电子式Cl- | D. | 质量数为37的氯原子${\;}_{37}^{17}$Cl |