题目内容
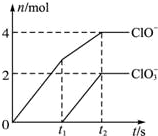 在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中有三种含氯元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线如图所示.已知,生成ClO3-的反应为:6Ca(OH)2+6Cl2═5CaCl2+Ca(ClO3)2+6H2O.
在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中有三种含氯元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线如图所示.已知,生成ClO3-的反应为:6Ca(OH)2+6Cl2═5CaCl2+Ca(ClO3)2+6H2O.试回答:
(1)0~t1时,Ca(OH)2与Cl2发生的离子方程式
(2)t2时Ca(ClO)2与Ca(ClO3)2的物质的量之和为
(3)若
| c(ClO-) | ||
n(Cl
|
考点:有关混合物反应的计算,离子方程式的有关计算
专题:
分析:(1)0~t1时,氢氧化钙与氯气反应生成氯化钙、次氯酸钙和水;
(2)由图可知,t2时氢氧化钙与氯气恰好反应,n(C1O-)=4mol,故n[Ca(ClO)2]=2mol,n(C1O3-)=2mol,故n[Ca(ClO3)2]=1mol,根据方程式6Ca(OH)2+6Cl2=5CaCl2+Ca(ClO3)2+6H2O和方程式2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O计算Ca(OH)2的物质的量,进而计算质量;
(2)若
=a,根据氯原子守恒可得:an(ClO3-)+n(ClO3-)+n(Cl-)=20,根据电子转移守恒可得:an(ClO3-)+5n(ClO3-)=n(Cl-),联立方程计算.
(2)由图可知,t2时氢氧化钙与氯气恰好反应,n(C1O-)=4mol,故n[Ca(ClO)2]=2mol,n(C1O3-)=2mol,故n[Ca(ClO3)2]=1mol,根据方程式6Ca(OH)2+6Cl2=5CaCl2+Ca(ClO3)2+6H2O和方程式2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O计算Ca(OH)2的物质的量,进而计算质量;
(2)若
| c(ClO-) | ||
n(Cl
|
解答:
解:(1)根据图象可知,0~t1时发生反应为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,反应的离子方程式为:Cl2+2OH-=ClO-+Cl-+H2O,
故答案为:Cl2+2OH-=ClO-+Cl-+H2O;
(2)由图可知,t2时氢氧化钙与氯气恰好反应,n(C1O-)=4mol,故n[Ca(ClO)2]=2mol,n(C1O3-)=2mol,则:n[Ca(ClO3)2]=1mol,所以Ca(ClO)2与Ca(ClO3)2的物质的量之和为3mol;
根据方程式6Ca(OH)2+6Cl2=5CaCl2+Ca(ClO3)2+6H2O和2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O可得Ca(OH)2的物质的量为:2mol×2+1mol×6=10mol,Ca(OH)2的质量为:10mol×74g=740g,
故答案为:3;740;
(2)由(2)可知,参加反应的氯气n(Cl2)=n[Ca(OH)2]=10mol,根据氯元素守恒可知,n(ClO-)+n(ClO3-)+n(Cl-)=2n(Cl2)=20mol,若
=a,则an(ClO3-)+n(ClO3-)=20-n(Cl-),根据电子转移守恒可得:an(ClO3-)+5n(ClO3-)=n(Cl-),两个方程联立解得:n(Cl-)=
,
故答案为:
.
故答案为:Cl2+2OH-=ClO-+Cl-+H2O;
(2)由图可知,t2时氢氧化钙与氯气恰好反应,n(C1O-)=4mol,故n[Ca(ClO)2]=2mol,n(C1O3-)=2mol,则:n[Ca(ClO3)2]=1mol,所以Ca(ClO)2与Ca(ClO3)2的物质的量之和为3mol;
根据方程式6Ca(OH)2+6Cl2=5CaCl2+Ca(ClO3)2+6H2O和2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O可得Ca(OH)2的物质的量为:2mol×2+1mol×6=10mol,Ca(OH)2的质量为:10mol×74g=740g,
故答案为:3;740;
(2)由(2)可知,参加反应的氯气n(Cl2)=n[Ca(OH)2]=10mol,根据氯元素守恒可知,n(ClO-)+n(ClO3-)+n(Cl-)=2n(Cl2)=20mol,若
| c(ClO-) | ||
n(Cl
|
| 10(a+5) |
| a+3 |
故答案为:
| 10(a+5) |
| a+3 |
点评:本题考查氯气性质、图象计算、离子方程式与化学方程式的书写、阅读获得信息的能力等,难度较大,读懂图象与信息判断发生的反应是解题的关键.

练习册系列答案
相关题目
春节燃放烟花后的烟雾中常含有CO、CO2、SO2等气体,所以烟花燃烧后的烟雾属于( )
| A、氧化物 | B、化合物 |
| C、纯净物 | D、混合物 |
下列说法正确的是( )
A、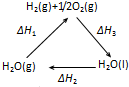 △H1=△H2+△H3 |
B、 在催化剂条件下,反应的活化能等于E1+E2 |
C、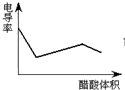 表示醋酸溶液滴定 NaOH 和氨水混合溶液的电导率变化曲线 |
D、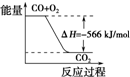 可表示由CO(g)生成CO2(g)的反应过程和能量关系 |
下列物质转化无法实现的是( )
A、Al2O3
| |||||
B、S
| |||||
C、Fe2O3
| |||||
D、MgCl2(aq)
|
氢氧化钙溶解度随温度的变化如表所示,下列说法错误的是( )
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 100 | 150 | 200 |
| 溶解度(g/100gH2O) | 0.18 | 0.17 | 0.16 | 0.15 | 0.14 | 0.11 | 0.092 | 0.074 | 0.034 | 0.012 |
| A、氢氧化钙的溶解是放热过程 |
| B、100℃时氢氧化钙的Kxp约等于4×10-6 |
| C、温度升高时氢氧化钙溶解速率加快 |
| D、100℃时pH=12的溶液中c(Ca2+)≤0.04mol?L-1 |

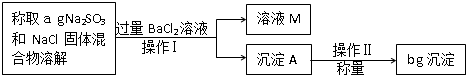
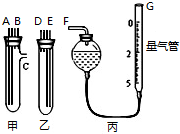 某校化学小组的同学开展测定Na2SO3和NaCl的固体混合物中Na2SO3质量分数的探究实验,他们提出下列实验方案:
某校化学小组的同学开展测定Na2SO3和NaCl的固体混合物中Na2SO3质量分数的探究实验,他们提出下列实验方案: