题目内容
11.(1)为了除去下列物质中的少量杂质(括号内为杂质),请在空白处填入适当的试剂,并写出相关反应的离子方程式或化学方程式.SiO2(CaCO3)盐酸;化学方程式为CaCO3+2HCl=CO2↑+H2O+CaCl2
KCl (KBr)适量氯气;离子方程式为Cl2+2Br-=Br2+2Cl-
(2)请写出实验室制氯气的化学方程式,并用双线桥标出电子转移的方向和数目.
MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O、
 .
.
分析 (1)二氧化硅不溶于盐酸,碳酸钙溶于盐酸,可用盐酸除去二氧化硅中的碳酸钙;氯气与溴化钾反应生成溴单质和氯化钾;
(2)实验室用浓盐酸与二氧化锰在加热条件下发生反应制备氯气,据此写出反应的化学方程式;Mn元素的化合价从+4价降为+2价,Cl元素从-1价升高为0价,据此通过双线桥分析此氧化还原反应.
解答 解:(1)SiO2(CaCO3):二氧化硅不溶于盐酸,碳酸钙溶于盐酸,可用盐酸除去二氧化硅中的碳酸钙,该反应的化学方程式为:CaCO3+2HCl=CO2↑+H2O+CaCl2;
KCl (KBr):氯气的氧化性大于溴单质,可用适量氯气除去氯化钾中的溴化钾,反应的离子方程式为:Cl2+2Br-=Br2+2Cl-,
故答案为:CaCO3+2HCl=CO2↑+H2O+CaCl2;Cl2+2Br-=Br2+2Cl-;
(2)实验室用浓盐酸与二氧化锰在加热条件下发生反应制备氯气,反应的方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,Mn元素的化合价从+4价降为+2价,Cl元素从-1价升高为0价,过双线桥分析此氧化还原反应为: ,其中MnO2做氧化剂,HCl做还原剂,
,其中MnO2做氧化剂,HCl做还原剂,
故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O、 .
.
点评 本题考查了离子方程式书写、物质的分离与提纯、氧化还原反应中电子转移的分析等知识,题目难度中等,明确物质分离与提纯的原则为解答关键,注意掌握分析氧化还原反应中电子转移方向和数目的方法.

练习册系列答案
相关题目
16.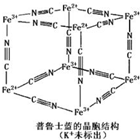 普鲁士蓝晶体结构如图所示(每两个立方体中,一个K+在其中一个立方体中心,另一个则无K+),下列说法正确的是( )
普鲁士蓝晶体结构如图所示(每两个立方体中,一个K+在其中一个立方体中心,另一个则无K+),下列说法正确的是( )
 普鲁士蓝晶体结构如图所示(每两个立方体中,一个K+在其中一个立方体中心,另一个则无K+),下列说法正确的是( )
普鲁士蓝晶体结构如图所示(每两个立方体中,一个K+在其中一个立方体中心,另一个则无K+),下列说法正确的是( )| A. | 化学式可以表示为KFe2(CN)6 | |
| B. | 每一个立方体中平均含有24个π键 | |
| C. | 普鲁士蓝不属于配位化合物 | |
| D. | 每个Fe3+周围与之相邻的Fe2+离子有12个 |
3.下列说法正确的是( )
| A. | 配制0.1mol/L CuSO4溶液100 mL,需称量CuSO4•5H2O 1.6g | |
| B. | 40g NaOH固体溶于1 L水,所得溶液的浓度为1 mol/L | |
| C. | 200mL 0.2mol/L MgCl2溶液中Cl-的个数为0.08NA | |
| D. | 从100mL 1mol/L H2SO4溶液取出10mL溶液,此溶液的浓度为0.1 mol/L |
20.下列溶液中有关微粒的物质的量浓度关系正确的是( )
| A. | NaHSO3和NaHCO3的中性混合溶液中(S和C均用R表示):c(Na+)=c(HRO3-)+c(RO32-) | |
| B. | 常温下将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后溶液中:c(Na+)>c(Cl-)>c(CH3COOH) | |
| C. | 常温下物质的量浓度相等的①(NH4)2CO3、②(NH4)2SO4、③(NH4)2Fe(SO4)2三种溶液中水的电离程度:①>③>② | |
| D. | 等体积等物质的量浓度的NaClO(aq)与NaCl(aq)中离子总数:N前>N后 |
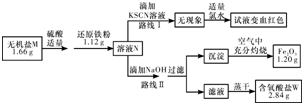
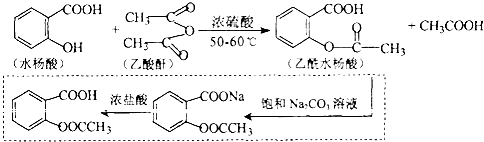


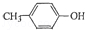 也能与乙酸酐发生类似反应,请写出化学反应方程式,可不写条件:
也能与乙酸酐发生类似反应,请写出化学反应方程式,可不写条件: .
.