题目内容
8.硫酸亚铁是重要的亚铁盐,在农业上用作农药,主要治小麦黑穗病,还可以用作除草剂;在工业上用于染色、制造蓝黑墨水和木材防腐等.(1)新制的绿矾(FeSO4•7H2O)是浅绿色的,但在空气中极易变成黄色或铁锈色的碱式硫酸铁[Fe(OH)SO4],写出该反应的化学方程式:4FeSO4•7H2O+O2=4Fe(OH)SO4+26H2O.
(2)已知FeSO4在不同条件下分解得到产物不同,可能是FeO和SO3,也可能是Fe2O3、SO3和SO2;SO3熔点是16.8℃,沸点是44.8℃.
某研究性学习小组拟用下列装置进行实验探究“在加热条件下FeSO4的分解产物”.
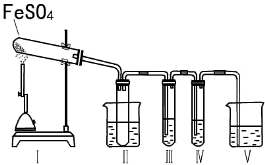
上述装置Ⅲ和Ⅳ用来检验气体产物.试回答下列问题:
①Ⅱ装置烧杯中水的温度应控制在 (选填“0℃、25℃、50℃”),装置Ⅱ的作用是防止产生倒吸(或“用作安全瓶”).
②装置Ⅲ中的试剂可以是C (选填序号,下同),现象是产生白色沉淀,则证明气体产物中含有SO3;装置Ⅳ中的试剂可以是B、E.
A.2mol/LNa2CO3溶液 B.品红溶液 C.0.5mol/L BaCl2溶液 D.0.5mol/LBa(NO3)2 E.0.01mol/L KMnO4溶液 F.淀粉碘化钾溶液
③装置V中试剂为NaOH溶液,发生反应的离子方程式为SO2+2OH-=SO32-+H2O.
④为了检验固体产物成分,取反应后的固体于试管中,加稀硫酸溶解,将所得溶液分成两份,进行如下实验:
| 操作步骤 | 预期实验现象 | 预期实验结论 |
| 向其中一份溶液中加入KSCN溶液(或硫氰化钾溶液) | 溶液变成血红色 | 固体中含有Fe2O3 |
| 向另一份溶液中滴加2滴黄色K3[Fe(CN)6]溶液 | 产生蓝色沉淀 | 固体中含有FeO |
分析 (1)亚铁离子易被氧化具有还原性,在空气中极易变成黄色或铁锈色的碱式硫酸铁[Fe(OH)SO4],原子守恒和电子守恒配平书写化学方程式;
(2)①安全瓶的作用是可以防止倒吸;当温度高于44.8°C时三氧化硫为气体状态;
②装置III是检验是否有三氧化硫,装置IV是检验是否有二氧化硫,根据二者的性质选择试剂;
③二氧化硫会污染空气,要用氢氧化钠溶液来处理尾气;
④检验三价铁离子用硫氰化钾溶液;检验二价铁离子用K3[Fe(CN)6]溶液;
⑤反应过程中FeSO4固体分解为二氧化硫、三氧化硫、FeO、Fe2O3,完全分解后得到11.2g固体为氧化铁和氧化亚铁,质量减少的为二氧化硫和三氧化硫的总质量,据此列方程组计算.
解答 解:(1)亚铁离子具有还原性,易被氧气氧化,反应方程式为:4FeSO4•7H2O+O2=4Fe(OH)SO4+26H2O,
故答案为:4FeSO4•7H2O+O2=4Fe(OH)SO4+26H2O;
(2)①SO3的沸点是44.8°C,当温度高于44.8°C时三氧化硫为气体状态,把试管浸泡在50℃的热水浴中能防止SO3液化或凝固,产生的气体极易和溶液反应时,会产生倒吸,所以装置II的试管能防止溶液倒吸入装置Ⅰ中(或安全瓶),
故答案为:50℃;防止产生倒吸(或“用作安全瓶”);
②装置III是检验是否有三氧化硫,可以选用氯化钡溶液,如果有白色沉淀生成说明有三氧化硫;装置IV是检验是否有二氧化硫,二氧化硫能使品红褪色,也能使酸性高锰酸钾溶液褪色,所以可以选用二者来检验二氧化硫;
故答案为:C;产生白色沉淀;B、E;
③二氧化硫会污染空气,所以要用氢氧化钠溶液来吸收剩余的二氧化硫,其反应的离子方程式为:SO2+2OH-=SO32-+H2O,故答案为:SO2+2OH-=SO32-+H2O;
④检验三价铁离子用硫氰化钾溶液,溶液变红色,证明有三价铁离子,进而说明固体产物中含有氧化铁;检验二价铁离子用K3[Fe(CN)6]溶液,溶液中生成蓝色沉淀,说明有二价铁离子,即证明固体产物中含有FeO;
故答案为:
| 操作步骤 | 预期实验现象 | 预期实验结论 |
| KSCN溶液(或硫氰化钾溶液) | 溶液变成血红色 | |
| 固体中含有FeO |
⑤反应过程中FeSO4固体分解为二氧化硫、三氧化硫、FeO、Fe2O3,完全分解后得到11.2g固体为氧化铁和氧化亚铁,质量减少的为二氧化硫和三氧化硫的总质量,
设生成的二氧化硫为xmol,三氧化硫为ymol,
根据硫元素守恒,则x+y=$\frac{22.8g}{152g/mol}$=0.15mol,
64x+80y=22.8g-11.2g=11.6g,
解得:x=0.025,y=0.125,
FeSO4固体分解,每生成1mol二氧化硫时硫元素得到2mol电子,每生成1molFe2O3时铁元素失去2mol电子,所以生成的二氧化硫与氧化铁的物质的量相同,
则Fe2O3的物质的量为0.025mol,其质量为0.025mol×160g/mol=4.0g,故质量分数为:$\frac{4.0g}{11.2g}$×100%=35.7%,
故答案为:35.7%.
点评 本题主要考查了学生亚铁离子和三价铁离子之间的相互转化,题目综合性较强,掌握基础是解题关键,题目难度较大.

| A. | H2A是弱酸 | |
| B. | 稀释0.1 mol/L H2A溶液,因电离平衡向右移动而导致c(H+)增大 | |
| C. | 在0.1 mol/L的H2A溶液中,c(H+)=0.12 mol/L | |
| D. | 若0.1 mol/L NaHA溶液中c(H+)=0.02 mol/L,则0.1 mol/L的H2A中c(H+)<0.12 mol/L |
(1)A的分子式为C7H10O5.
(2)又知1molA能与足量的NaHCO3溶液反应生成22.4LCO2(标准状况),与足量的金属钠反应得到44.8LH2(标准状况),还能与Br2按物质的量之比1:1完全加成,根据上述信息,将A分子中含氧官能团的名称及数目填入下表(可不填满,也可补充).
| 含氧官能团名称 | |||
| 含氧官能团数目 |
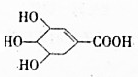 ”,你认为这种结构是否存在:是,该物质在一定条件下能(填“能”或“不能”)发生分子内的酯化反应,作出此判断的理由是含有羟基和羧基.
”,你认为这种结构是否存在:是,该物质在一定条件下能(填“能”或“不能”)发生分子内的酯化反应,作出此判断的理由是含有羟基和羧基. | A. | 盐酸能导电,所以盐酸是电解质 | |
| B. | 纯碱的化学式:NaOH | |
| C. | 碳酸钾的电离方程式:K2CO3=2K+1+CO3-2 | |
| D. | 氯离子的结构示意图为: |

 .
. 根据所学,回答下列问题:
根据所学,回答下列问题: <
<  (填“>”“<”或“=”,下同)
(填“>”“<”或“=”,下同) <
<
 >CH3COOH.
>CH3COOH.
 +R′OH→
+R′OH→ +HCl
+HCl
 .
. .
. 的路线.
的路线. .
.