题目内容
18.下列说法正确的是( )| A. | 盐酸能导电,所以盐酸是电解质 | |
| B. | 纯碱的化学式:NaOH | |
| C. | 碳酸钾的电离方程式:K2CO3=2K+1+CO3-2 | |
| D. | 氯离子的结构示意图为: |
分析 A.盐酸为混合物,混合物既不是电解质,也不是非电解质;
B.纯碱为碳酸钠,氢氧化钠为火碱、烧碱、苛性钠;
C.钾离子和碳酸根离子的表示方法错误;
D.氯离子的核电荷数为17,核外电子总数为18,最外层满足8电子稳定结构.
解答 解:A.盐酸为混合物,单质和混合物不属于电解质和非电解质,故A错误;
B.纯碱为碳酸钠,其化学式为:Na2CO3,而NaOH的俗名为烧碱、苛性钠,故B错误;
C.碳酸钾为强电解质,在溶液中完全电离,其正确的电离方程式为:K2CO3=2K++CO32-,故C错误;
D.氯离子的核电荷数为17,最外层达到8电子稳定结构,其离子结构示意图为: ,故D正确;
,故D正确;
故选D.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电离方程式、离子结构示意图、电解质与非电解质等知识,明确常见化学用语的概念及书写原则为解答关键,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
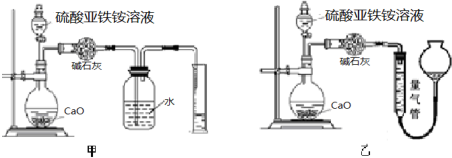
8.硫酸亚铁是重要的亚铁盐,在农业上用作农药,主要治小麦黑穗病,还可以用作除草剂;在工业上用于染色、制造蓝黑墨水和木材防腐等.
(1)新制的绿矾(FeSO4•7H2O)是浅绿色的,但在空气中极易变成黄色或铁锈色的碱式硫酸铁[Fe(OH)SO4],写出该反应的化学方程式:4FeSO4•7H2O+O2=4Fe(OH)SO4+26H2O.
(2)已知FeSO4在不同条件下分解得到产物不同,可能是FeO和SO3,也可能是Fe2O3、SO3和SO2;SO3熔点是16.8℃,沸点是44.8℃.
某研究性学习小组拟用下列装置进行实验探究“在加热条件下FeSO4的分解产物”.
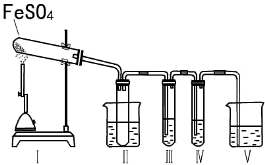
上述装置Ⅲ和Ⅳ用来检验气体产物.试回答下列问题:
①Ⅱ装置烧杯中水的温度应控制在 (选填“0℃、25℃、50℃”),装置Ⅱ的作用是防止产生倒吸(或“用作安全瓶”).
②装置Ⅲ中的试剂可以是C (选填序号,下同),现象是产生白色沉淀,则证明气体产物中含有SO3;装置Ⅳ中的试剂可以是B、E.
A.2mol/LNa2CO3溶液 B.品红溶液 C.0.5mol/L BaCl2溶液 D.0.5mol/LBa(NO3)2 E.0.01mol/L KMnO4溶液 F.淀粉碘化钾溶液
③装置V中试剂为NaOH溶液,发生反应的离子方程式为SO2+2OH-=SO32-+H2O.
④为了检验固体产物成分,取反应后的固体于试管中,加稀硫酸溶解,将所得溶液分成两份,进行如下实验:
⑤若用22.8g FeSO4固体做实验,完全分解后,得到11.2g固体,其中Fe2O3的质量分数=35.7%(精确到0.1%)
(1)新制的绿矾(FeSO4•7H2O)是浅绿色的,但在空气中极易变成黄色或铁锈色的碱式硫酸铁[Fe(OH)SO4],写出该反应的化学方程式:4FeSO4•7H2O+O2=4Fe(OH)SO4+26H2O.
(2)已知FeSO4在不同条件下分解得到产物不同,可能是FeO和SO3,也可能是Fe2O3、SO3和SO2;SO3熔点是16.8℃,沸点是44.8℃.
某研究性学习小组拟用下列装置进行实验探究“在加热条件下FeSO4的分解产物”.

上述装置Ⅲ和Ⅳ用来检验气体产物.试回答下列问题:
①Ⅱ装置烧杯中水的温度应控制在 (选填“0℃、25℃、50℃”),装置Ⅱ的作用是防止产生倒吸(或“用作安全瓶”).
②装置Ⅲ中的试剂可以是C (选填序号,下同),现象是产生白色沉淀,则证明气体产物中含有SO3;装置Ⅳ中的试剂可以是B、E.
A.2mol/LNa2CO3溶液 B.品红溶液 C.0.5mol/L BaCl2溶液 D.0.5mol/LBa(NO3)2 E.0.01mol/L KMnO4溶液 F.淀粉碘化钾溶液
③装置V中试剂为NaOH溶液,发生反应的离子方程式为SO2+2OH-=SO32-+H2O.
④为了检验固体产物成分,取反应后的固体于试管中,加稀硫酸溶解,将所得溶液分成两份,进行如下实验:
| 操作步骤 | 预期实验现象 | 预期实验结论 |
| 向其中一份溶液中加入KSCN溶液(或硫氰化钾溶液) | 溶液变成血红色 | 固体中含有Fe2O3 |
| 向另一份溶液中滴加2滴黄色K3[Fe(CN)6]溶液 | 产生蓝色沉淀 | 固体中含有FeO |
9.下列关于乙醇的说法不正确的是( )
| A. | 可用粮食发酵制取 | B. | 可由乙烯通过加成反应制取 | ||
| C. | 与乙醛互为同分异构体 | D. | 通过取代反应可以制取乙酸乙酯 |
6.下列关于物质性质变化的比较中,不正确的是( )
| A. | 碱性强弱:KOH>NaOH>LiOH | B. | 原子半径大小:Na>S>O | ||
| C. | 酸性强弱:HIO4>HBrO4>HClO4 | D. | 金属性强弱:Na>Mg>Al |
13.下列说法正确的是( )
| A. | 葡萄糖可以水解成乙醇 | B. | 石油裂解气产物可用于制备塑料 | ||
| C. | CH2═CH2和CH3CH2Cl 都属于烃 | D. | 蛋白质、油脂均属高分子化合物 |
10.下列微粒半径由大到小的排列是( )
| A. | P3-、S2-、Cl- | B. | Cl-、S2-、O2- | C. | Ca、Mg、Na | D. | K+、Cl-、S2- |
7.能证明乙醇分子中含有一个羟基的事实是( )
| A. | 1mol乙醇完全燃烧生成3mol水 | |
| B. | 乙醇能与水以任意比例互溶 | |
| C. | 乙醇沸点较高 | |
| D. | 0.1mol乙醇与足量金属钠反应生成0.05molH2 |