题目内容
11.获得中科院“百人计划”和“863”计划支持的环境友好型铝碘电池是以AlI3溶液为电解质溶液,以金属铝和附有碘单质的石墨为电极形成的原电池.已知电池总反应为2Al+3I2═2AlI3.下列说法不正确的是( )| A. | 电池工作时,溶液中的铝离子向正极移动 | |
| B. | 该电池可能是一种可充电的二次电池 | |
| C. | 消耗相同质量金属时,用锂做负极时,产生电子的物质的量比铝多 | |
| D. | 该电池负极的电极反应为:Al-3e-═Al3+ |
分析 由电池总反应为2Al+3I2═2AlI3,Al元素的化合价升高、I元素的化合价降低,则Al为负极,发生氧化反应,阳离子向正极移动,以此来解答.
解答 解:A.原电池工作时,阳离子向正极移动,故A正确;
B.该反应的逆过程不能发生,所以该电池为一次电池,故B错误;
C.因Al的摩尔质量为27g/mol,由$\frac{m}{M}$×失去的电子数可知,消耗相同质量金属时,用锂做负极时,产生电子的物质的量比铝多,故C正确;
D.因Al元素的化合价升高,则电池负极的电极反应为Al-3e-═Al3+,故D正确.
故选B.
点评 本题考查化学电源新型电池,注意发生的电池反应与氧化还原反应的关系即可解答,明确发生的电极反应及原电池工作原理来解答,题目难度中等.

练习册系列答案
相关题目
2.下列实验的反应原理用离子方程式表示正确的是( )
| A. | 明矾净水:Al3++3H2O=Al(OH)3↓+3H+ | |
| B. | 用过量氨水吸收工业尾气中的SO2:2NH3•H2O+SO2=2NH4++SO32-+H2O | |
| C. | 用CuCl2溶液做导电实验,灯泡发光:CuCl2$\frac{\underline{\;通电\;}}{\;}$Cu2++2C1- | |
| D. | 用高锰酸钾标准溶液滴定草酸:2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O |
19.下列说法不正确的是( )
| A. | 丁达尔效应可用于鉴别胶体和溶液 | |
| B. | 胶体粒子的直径在1~100 nm之间 | |
| C. | 胶体一定是混合物 | |
| D. | 将FeCl3稀溶液溶于冷水即可制得Fe(OH)3胶体 |
6.如图的烧杯中盛的都是海水,铁在其中被腐蚀的速率由快到慢的顺序为( )
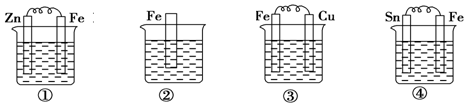

| A. | ③④②① | B. | ③④①② | C. | ④②①③ | D. | ②①③④ |
16.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 常温下,1 mol•L-1的NH4NO3溶液中含有氮原子的数目为2 NA | |
| B. | 22.4L氯气通入足量氢氧化钠溶液中充分反应,转移的电子数为NA | |
| C. | 标准状况下,5.6 L四氯化碳含有的分子数为0.25NA | |
| D. | 4.6gNa完全转化成Na2O和Na2O2的混合物,生成物中阴离子总数为0.1NA |
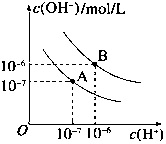 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示: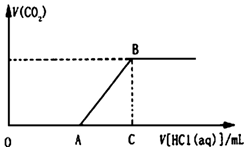 向100mL某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2,使其充分反应.在上述所得溶液中,逐滴缓慢滴加1mol•L-1的盐酸,所得气体(不考虑溶解)的体积与滴加盐酸的体积关系如图(其中点A是线段OC上的动点):
向100mL某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2,使其充分反应.在上述所得溶液中,逐滴缓慢滴加1mol•L-1的盐酸,所得气体(不考虑溶解)的体积与滴加盐酸的体积关系如图(其中点A是线段OC上的动点):
 CH3COOCH2CH3+H2O;反应类型酯化反应.
CH3COOCH2CH3+H2O;反应类型酯化反应.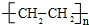 ;反应类型加聚反应.
;反应类型加聚反应.