题目内容
13.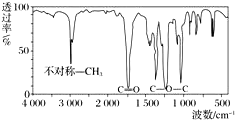 取8.8g有机物X,完全燃烧后只生成7.2g水和 8.96L CO2(标准状况),已知该有机物的蒸气对氢气的相对密度为44,其红外光谱图如图.关于X的说法错误的是( )
取8.8g有机物X,完全燃烧后只生成7.2g水和 8.96L CO2(标准状况),已知该有机物的蒸气对氢气的相对密度为44,其红外光谱图如图.关于X的说法错误的是( )| A. | 其化学式为C4H8O2 | |
| B. | 其满足右侧图象的酯有3种 | |
| C. | 鉴定该有机物的结构可用红外光谱或核磁共振氢谱 | |
| D. | 若结构为CH3COOCH2CH3,其核磁共振氢谱中有3个峰 |
分析 有机物X的蒸气密度是相同条件下H2密度的44倍,则该有机物的相对分子质量为44×2=88,X的物质的量为$\frac{8.8g}{88g/mol}$=0.1mol,n(H2O)=$\frac{7.2g}{18g/mol}$=0.4mol,所以n(H)=2n(H2O)=0.8mol,n(CO2)=$\frac{8.96L}{22.4L/mol}$=0.4mol,故n(C)=n(CO2)=0.4mol,X分子中N(C)=$\frac{0.4mol}{0.1mol}$=4、N(H)=$\frac{0.8mol}{0.1mol}$=8,故N(O)=$\frac{88-12×4-8}{16}$=2,则有机物X的分子式为C4H8O2,根据红外光谱图可知,有机物含有不对称甲基、含有C=O、C-O-C结构,结合选项判断.
解答 解:A.有机物X的蒸气密度是相同条件下H2密度的44倍,则该有机物的相对分子质量为44×2=88,X的物质的量为$\frac{8.8g}{88g/mol}$=0.1mol,n(H2O)=$\frac{7.2g}{18g/mol}$=0.4mol,所以n(H)=2n(H2O)=0.8mol,n(CO2)=$\frac{8.96L}{22.4L/mol}$=0.4mol,故n(C)=n(CO2)=0.4mol,X分子中N(C)=$\frac{0.4mol}{0.1mol}$=4、N(H)=$\frac{0.8mol}{0.1mol}$=8,故N(O)=$\frac{88-12×4-8}{16}$=2,则有机物X的分子式为C4H8O2,故A正确;
B.根据红外光谱图可知,有机物含有不对称甲基、含有C=O、C-O-C结构,X若属于酯,可能的结构简式有:CH3COOCH2CH3,CH3CH2COOCH3,故B错误;
C.红外光谱可以确定含有的官能团与基团,核磁共振氢谱可以确定含有H原子种类,故C正确;
D.若结构为CH3COOCH2CH3,分子中有3种化学环境不同的氢,其核磁共振氢谱中有3个峰,故D正确,
故选:B.
点评 本题考查有机物分子式与结构式的确定、限制条件同分异构体书写,注意掌握燃烧法利用守恒确定有机物分子式.

 名校课堂系列答案
名校课堂系列答案| A. | PCl5的分解率大于a% | |
| B. | PCl5的分解率小于a% | |
| C. | 达到平衡后正逆反应速率比原平衡状态时大 | |
| D. | 达到平衡后正逆反应速率比原平衡状态时小 |
| A. | $\frac{2}{5}$ mol | B. | $\frac{11}{5}$ mol | C. | $\frac{1}{5}$ mol | D. | $\frac{1}{3}$ mol |
 甲溶液中含Aa+离子浓度为0.10mol/L,乙溶液含Bb-离子浓度为0.35mol/L,取不同体积甲、乙两溶液的物质的量如图所示.则沉淀物的化学式为( )
甲溶液中含Aa+离子浓度为0.10mol/L,乙溶液含Bb-离子浓度为0.35mol/L,取不同体积甲、乙两溶液的物质的量如图所示.则沉淀物的化学式为( )| A. | A2B3 | B. | A3B2 | C. | AB2 | D. | A2 |
 )是一种重要的化工原料和医药中间体,实验室合成三苯甲醇的流程如图1所示,装置如图2所示.
)是一种重要的化工原料和医药中间体,实验室合成三苯甲醇的流程如图1所示,装置如图2所示.
已知:(I)格氏试剂容易水解:

(Ⅱ)相关物质的物理性质如下:
| 物质 | 熔点 | 沸点 | 溶解性 |
| 三苯甲醇 | 164.2℃ | 380℃ | 不溶于水,溶于乙醇、乙醚等有机溶剂 |
| 乙醚 | -116.3℃ | 34.6℃ | 微溶于水,溶于乙醇、苯等有机溶剂 |
| 溴苯 | -30.7℃ | 156.2℃ | 不溶于水,溶于乙醇、乙醚等有机溶剂 |
请回答以下问题:
(1)装置中玻璃仪器B的名称为冷凝管;装有无水CaCl2的仪器A的作用是防止空气中的水蒸气进入装置,避免格氏试剂水解.
(2)装置中滴加液体未用普通分液漏斗而用滴液漏斗的作用是平衡压强,使漏斗内液体顺利滴下;制取格氏试剂时要保持温度约为40℃,可以采用水浴加热方式.
(3)制得的三苯甲醇粗产品经过初步提纯,仍含有氯化铵杂质,可以设计如下提纯方案:

其中,洗涤液最好选用a(填字母序号).
a.水 b.乙醚 c.乙醇 d.苯
检验产品已经洗涤干净的操作为取少量最后一次洗涤液于试管中,滴加硝酸银溶液,若无沉淀生成,则已洗涤干净,反之则未洗涤干净.
(4)纯度测定:称取2.60g产品,配成乙醚溶液,加入足量金属钠(乙醚与钠不反应),充分反应后,测得生成的气体在标准状况下的体积为100.80mL.则产品中三苯甲醇的质量分数为90%.
| A. | 由SiO2不能与水反应生成H2SiO3,可知SiO2不是H2SiO3的酸酐 | |
| B. | 由SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,可知碳的非金属性大于硅 | |
| C. | CO2通入Na2SiO3溶液产生白色沉淀,可知酸性H2CO3>H2SiO3 | |
| D. | SiO2可与NaOH溶液反应,也可与氢氟酸反应,可知SiO2为两性氧化物 |
| A. | 做衣服的棉和麻均与淀粉互为同分异构体 | |
| B. | 燃料的脱硫脱氮、SO2的回收利用和NOx的催化转化都是减少酸雨产生的措施 | |
| C. | 铁在潮湿的空气中放置,易发生化学腐蚀而生锈 | |
| D. | 用含有橙色的酸性重铬酸钾的仪器检验酒后驾车,利用了乙醇的氧化性 |
| A. | 0.1mol•L-1的CH3COOH溶液的pH=2 | B. | CH3COOH溶液中含有CH3COOH分子 | ||
| C. | CH3COOH能与NaOH发生中和反应 | D. | 常温下CH3COONa溶液的pH=8 |