题目内容
16.一定温度下,在一密闭容器中加入1molPCl5,发生反应PCl5(g)?PCl3(g)+Cl2 (g)充分反应平衡后,测得PCl5的分解率为a%,此时,再向密闭容器中加入1mol PCl5,充分反应,再次平衡后,下列有关说法正确的是( )| A. | PCl5的分解率大于a% | |
| B. | PCl5的分解率小于a% | |
| C. | 达到平衡后正逆反应速率比原平衡状态时大 | |
| D. | 达到平衡后正逆反应速率比原平衡状态时小 |
分析 反应PCl5(g)?PCl3(g)+Cl2(g)为正反应气体体积增大的可逆反应,1.0molPCl5充入体积不变的密闭容器中,可以假设放入另一相同容积的密闭容器中,相同条件下达到平衡时,与上一平衡状态完全相同,再压入一个容器中,平衡逆向移动,据此分析.
解答 解:反应PCl5(g)?PCl3(g)+Cl2(g)为正反应气体体积增大的可逆反应,1.0molPCl5充入体积不变的密闭容器中,可以假设放入另一相同容积的密闭容器中,相同条件下达到平衡时,与上一平衡状态完全相同,再压入一个容器中,相当于增大压强,平衡逆向移动,而各组分的浓度变大,所以PCl5的分解率小于a%,再次达到平衡后正逆反应速率比原平衡状态时大,
故选:BC.
点评 本题考查化学平衡的移动,题目难度中等,注意假设法的利用,相当于在原平衡的基础上增大压强,平衡逆向移动,但各给分的浓度都变大.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案
相关题目
7.下列选项表示物质结构的化学用语或模型正确的是( )
| A. | 甲烷分子的比例模型: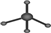 | B. | 乙烯的结构简式:CH2CH2 | ||
| C. | 醛基的电子式: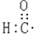 | D. | 甲醛的结构式: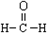 |
4.将过量的气体通入到一种溶液中,一定能产生沉淀的是( )
①二氧化硫通入到硝酸钡溶液中
②二氧化碳通入到偏铝酸钠溶液中
③二氧化碳通入到氯化钙溶液中
④氨气通入到氯化镁溶液中.
①二氧化硫通入到硝酸钡溶液中
②二氧化碳通入到偏铝酸钠溶液中
③二氧化碳通入到氯化钙溶液中
④氨气通入到氯化镁溶液中.
| A. | 只有①②③ | B. | 只有①② | C. | 只有②③ | D. | 只有①②④ |
11.氯气溶于水发生反应,写出其化学方程式Cl2+H2O═HCl+HClO.
某学生为了探究氯水的成分,请你与他一起完成探究过程,并书写实验报告.
某学生为了探究氯水的成分,请你与他一起完成探究过程,并书写实验报告.
| 实验步骤 | 操作方法 | 实验现象 | 结论或解释 |
| 1 | 观察氯水的颜色 | 含有Cl2 | |
| 2 | 有无色气体产生 | 含有H+ | |
| 3 | 取少量氯水于试管中,加入稀硝酸酸化的硝酸银溶液 | 有白色沉淀生成 | |
| 4 | 取少量氯水于试管中,放入红色布条 |
8.硫铁矿(主要成分为FeS2)在空气中高温煅烧可得SO2和Fe2O3,是我国硫酸工业的主要原料.某化学研究小组拟在实验室利用硫铁矿煅烧所得残渣(主要成分为Fe2O3,还含少量的SiO2,Al2O3,其余杂质不参予反应),制取颜料铁红(Fe2O3).设计工艺流程如下: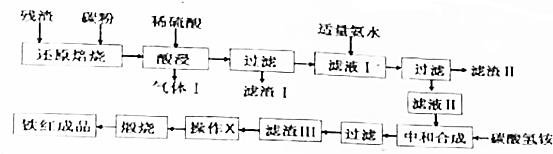
查阅资料:
Ⅰ部分金属离子发生沉淀的pH:
Ⅱ“中和合成”时发生的主要反应为:Fe2++2HCO3-=FeCO3↓+CO2↑+H2O.
请根据以上工艺流程及提供的信息,回答下列问题:
(1)气体Ⅰ的主要成分为H2(填化学式,下同);滤渣Ⅱ的主要成分为Al(OH)3、Fe(OH)3.
(2)操作X为洗涤(填操作名称).
(3)向滤液Ⅰ中加入适量氨水,其目的是调节溶液的pH到5.4~7.5之间.
(4)在“酸浸”过程中,若在空气中“酸浸”时间过长,溶液中Fe2+含量将下降,其原因是(用离子方程式表示):4Fe2++O2+4H+═4Fe3++2H2O.
(5)为测定滤液Ⅰ中的Fe2+的含量,实验室中常用酸性高锰酸钾溶液进行滴定,该反应的离子方程式为:MnO4-+5Fe2++8H+═Mn2++5Fe3++4H2O;取20.00mL滤液Ⅰ于锥形瓶中,用0.1mol/L酸性高锰酸钾溶液滴定到终点时消耗了标准酸性高锰酸钾溶液12.00mL,则滤液Ⅰ中c(Fe2+)=0.3mol/L.

查阅资料:
Ⅰ部分金属离子发生沉淀的pH:
| 金属离子 | Fe3+ | Al3+ | Fe2+ |
| 开始沉淀的pH | 2.2 | 3.1 | 7.5 |
| 完全沉淀的pH | 3.5 | 5.4 | 9.5 |
请根据以上工艺流程及提供的信息,回答下列问题:
(1)气体Ⅰ的主要成分为H2(填化学式,下同);滤渣Ⅱ的主要成分为Al(OH)3、Fe(OH)3.
(2)操作X为洗涤(填操作名称).
(3)向滤液Ⅰ中加入适量氨水,其目的是调节溶液的pH到5.4~7.5之间.
(4)在“酸浸”过程中,若在空气中“酸浸”时间过长,溶液中Fe2+含量将下降,其原因是(用离子方程式表示):4Fe2++O2+4H+═4Fe3++2H2O.
(5)为测定滤液Ⅰ中的Fe2+的含量,实验室中常用酸性高锰酸钾溶液进行滴定,该反应的离子方程式为:MnO4-+5Fe2++8H+═Mn2++5Fe3++4H2O;取20.00mL滤液Ⅰ于锥形瓶中,用0.1mol/L酸性高锰酸钾溶液滴定到终点时消耗了标准酸性高锰酸钾溶液12.00mL,则滤液Ⅰ中c(Fe2+)=0.3mol/L.
13.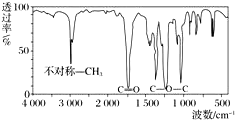 取8.8g有机物X,完全燃烧后只生成7.2g水和 8.96L CO2(标准状况),已知该有机物的蒸气对氢气的相对密度为44,其红外光谱图如图.关于X的说法错误的是( )
取8.8g有机物X,完全燃烧后只生成7.2g水和 8.96L CO2(标准状况),已知该有机物的蒸气对氢气的相对密度为44,其红外光谱图如图.关于X的说法错误的是( )
 取8.8g有机物X,完全燃烧后只生成7.2g水和 8.96L CO2(标准状况),已知该有机物的蒸气对氢气的相对密度为44,其红外光谱图如图.关于X的说法错误的是( )
取8.8g有机物X,完全燃烧后只生成7.2g水和 8.96L CO2(标准状况),已知该有机物的蒸气对氢气的相对密度为44,其红外光谱图如图.关于X的说法错误的是( )| A. | 其化学式为C4H8O2 | |
| B. | 其满足右侧图象的酯有3种 | |
| C. | 鉴定该有机物的结构可用红外光谱或核磁共振氢谱 | |
| D. | 若结构为CH3COOCH2CH3,其核磁共振氢谱中有3个峰 |
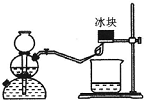 (1)下面所列的是中学化学实验室中几种常见的仪器:容量瓶、酸式滴定管、碱式滴定管、温度计、量筒、托盘天平、普通漏斗、玻璃棒、烧杯.
(1)下面所列的是中学化学实验室中几种常见的仪器:容量瓶、酸式滴定管、碱式滴定管、温度计、量筒、托盘天平、普通漏斗、玻璃棒、烧杯.