题目内容
18.已知樟脑(C10H16O)的结构如图,下列4式中与樟脑不属于同分异构体的是( )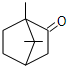
| A. |  | B. | 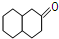 | C. |  | D. |  |
分析 同分异构体指分子式相同结构不同的化合物,据此物质的组成与化学式判断.
解答 解: 分子式为C10H16O.
分子式为C10H16O.
A. 分子式为C10H16O,分子式相同,结构不同,互为同分异构体,故A错误;
分子式为C10H16O,分子式相同,结构不同,互为同分异构体,故A错误;
B. 分子式为C10H16O,分子式相同,结构不同,互为同分异构体,故B错误;
分子式为C10H16O,分子式相同,结构不同,互为同分异构体,故B错误;
C. 分子式为C10H16O,分子式相同,结构不同,互为同分异构体,故C错误;
分子式为C10H16O,分子式相同,结构不同,互为同分异构体,故C错误;
D. 分子式为C10H18O,不互为同分异构体,故D正确.
分子式为C10H18O,不互为同分异构体,故D正确.
故选D.
点评 本题主要考查有机物同分异构体的书写,题目难度中等,注意掌握同分异构体的概念及求算方法.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
9.下列有关物质的应用说法正确的是( )
| A. | 碳酸钠可作胃酸的中和剂 | B. | SiO2可用于制造太阳能电池 | ||
| C. | 铁经常用作红色油漆和涂料 | D. | 生石灰用作食品抗氧化剂 |
6.反应A(g)+B(g)?2C(g);△H<0,达到平衡时,下列说法正确的是( )
| A. | 其他条件不变,减小容器体积,平衡不移动 | |
| B. | 其他条件不变,增大c(A),A的转化率增大 | |
| C. | 降低温度,v正增大,v逆减小 | |
| D. | v正(A)═2v逆(C) |
3.下列有关化学基本概念的依据正确的是( )
| A. | 同素异形体:是否由同一种原子构成 | |
| B. | 纯净物和混合物:是否只含一种元素 | |
| C. | 电解质和非电解质:溶于水或熔融状态下能否导电 | |
| D. | 氧化还原反应:元素化合价是否变化 |
10.已知部分弱酸的电离平衡常数如下表:
下列离子方程式正确的是( )
| 弱酸 | 醋酸 | 次氯酸 | 碳酸 | 亚硫酸 |
| 电离平衡常数 (25℃) | Ka=1.75ⅹ10-5 | Ka=2.98ⅹ10-8 | Ka1=4.3ⅹ10-7 Ka2=5.61ⅹ10-11 | Ka1=1.54ⅹ10-2 Ka2=1.02ⅹ10-7 |
| A. | 少量的CO2通入NaClO溶液中:CO2+H2O+2ClO-═CO32-+2HClO | |
| B. | 少量的SO2通入Na2CO3溶液中:SO2+H2O+2CO32-═SO32-+2HCO3- | |
| C. | 少量的SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO | |
| D. | 相同浓度的NaHCO3溶液与NaHSO3溶液等体积混合:H++HCO3-═CO2↑+2H2O |
7.下表是元素周期表的一部分,按要求完成各小题.
(1)元素①的元素符号:Na
(2)元素⑧的单质电子式
(3)元素⑤的原子结构示意图
(4)化学性质最不活泼的元素⑩(填元编号,下同),非金属性最强的元素是⑪.金属
性最强的单质②.
(5)①③⑤三种元素的最高价氧化物水化物中,碱性最强的NaOH.①③⑤三种元素的原子半径由大到小的顺序为Na>Mg>Al.
(6)某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐与水,该元素的最高价氧化物和盐酸反应的化学方程式为Al2O3+6HCl=2AlCl3+3H2O,与氢氧化钠溶液反应的化学方程式Al2O3+2NaOH=2NaAlO2+H2O.
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅥⅠA | 0 | |
| 2 | ⑥ | ⑦ | ⑪ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)元素⑧的单质电子式

(3)元素⑤的原子结构示意图

(4)化学性质最不活泼的元素⑩(填元编号,下同),非金属性最强的元素是⑪.金属
性最强的单质②.
(5)①③⑤三种元素的最高价氧化物水化物中,碱性最强的NaOH.①③⑤三种元素的原子半径由大到小的顺序为Na>Mg>Al.
(6)某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐与水,该元素的最高价氧化物和盐酸反应的化学方程式为Al2O3+6HCl=2AlCl3+3H2O,与氢氧化钠溶液反应的化学方程式Al2O3+2NaOH=2NaAlO2+H2O.
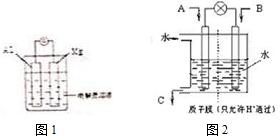 电能与化学能之间的转化具有重要的使用价值.
电能与化学能之间的转化具有重要的使用价值.