题目内容
12.某合作学习小组讨论辨析以下说法:①漂白粉和水玻璃都是混合物
②SO2和氯水都有漂白性,二者混合后漂白性更强,
③冰和干冰既是纯净物又是化合物
④淀粉和纤维素通式均为(C6H10O5)n,但二者不是同分异构体;
⑤酸性氧化物一定是非金属氧化物
⑥SiO2和硅都是电的良导题,
上述说法正确的是( )
| A. | ①②③ | B. | ①②⑤ | C. | ③⑤⑥ | D. | ①③④ |
分析 ①混合物是由两种以上物质组成的物质;
②等物质的量的二氧化硫与反应生成盐酸和硫酸;
③根据冰和干冰的成分考虑;
④同分异构体是分子式相同结构式不同的化合物;
⑤酸性氧化物不一定是非金属氧化物;
⑥二氧化硅不导电.
解答 解:①漂白粉含有氯化钙和次氯酸钙,水玻璃为硅酸的水溶液,都是混合物,故正确;
②等物质的量的二氧化硫与反应生成盐酸和硫酸,盐酸和硫酸不具有漂白性,故错误;
③冰是固态的水,干冰是固态二氧化碳,所以它们既是纯净物又是化合物,故正确;
④同分异构体是分子式相同结构式不同的化合物,淀粉和纤维素虽具有相同的表示式,但n不同,则分子式不同,故不是同分异构体,故正确;
⑤酸性氧化物不一定是非金属氧化物,例如Mn2O7金属氧化物但是酸性氧化物,故错误;
⑥二氧化硅不导电,是绝缘体,故错误;
故选:D.
点评 本题考查了元素化合物知识,熟悉化合物、纯净物、混合物、酸性氧化物的概念及常见物质的性质是解题关键,题目难度不大,注意对基础知识的积累.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.313K时,水的离子积Kw=2.9×10-14,则在313K时,c(H+)=10-7mol/L的溶液( )
| A. | 呈酸性 | B. | 呈中性 | C. | 呈碱性 | D. | 无法判断 |
3.足量下列物质能与等质量的氧化铝反应,且消耗溶质物质的量最少的是( )
| A. | 氢氧化钠溶液 | B. | 稀硫酸 | C. | 稀盐酸 | D. | 氨水 |
20.如果在容量瓶上刻上“20℃100mL”,需要使用的试剂是( )
| A. | 烧碱 | B. | 氢氟酸溶液 | C. | 盐酸 | D. | 碳酸钠溶液 |
5.关于用水制取二级能源氢气,以下研究方向不正确的是( )
| A. | 设法将太阳光聚焦,产生高温,使水分解产生氢气 | |
| B. | 寻找特殊化学物质,使水分解产生氢气,同时释放能量 | |
| C. | 寻找特殊化学物质,用于开发廉价能源以分解水制取氢气 | |
| D. | 构成水的氢气和氧气都是可燃烧的物质,因此可研究在水不分解的情况下,使氢能成为二级能源 |
2.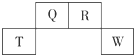 短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中W的原子核内质子数与核外最外层电子数之比为8:3,下列说法正确的是( )
短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中W的原子核内质子数与核外最外层电子数之比为8:3,下列说法正确的是( )
 短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中W的原子核内质子数与核外最外层电子数之比为8:3,下列说法正确的是( )
短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中W的原子核内质子数与核外最外层电子数之比为8:3,下列说法正确的是( )| A. | Q的最高价氧化物对应水化物的酸性大于R的最高价氧化物对应水化物的酸性 | |
| B. | T的离子半径大于W的离子半径 | |
| C. | 元素T形成单质的还原性大于元素W形成单质的还原性 | |
| D. | 在R的最高价氧化物对应水化物的浓溶液中单质T不溶解,说明未发生化学反应 |
3.在反应2Na+2H2O═2NaOH+H2↑中,生成1mol H2时转移电子数目为( )
| A. | 2NA | B. | NA | C. | 1.5NA | D. | 0.5 NA |