题目内容
2.313K时,水的离子积Kw=2.9×10-14,则在313K时,c(H+)=10-7mol/L的溶液( )| A. | 呈酸性 | B. | 呈中性 | C. | 呈碱性 | D. | 无法判断 |
分析 313K时,水的Kw=3.0×10-14,在313K时,c(H+)=10-7 mol/L的溶液中c(OH-)=$\frac{{k}_{w}}{c({H}^{+})}$,根据c(H+)、c(OH-)的相对大小判断溶液酸碱性,据此分析解答.
解答 解:313K时,水的Kw=3.0×10-14,在313K时,c(H+)=10-7 mol/L的溶液中c(OH-)=$\frac{{k}_{w}}{c({H}^{+})}$=$\frac{3.0×1{0}^{-14}}{1{0}^{-7}}$=3.0×10-7 mol/L>c(H+)=10-7 mol/L,则溶液呈碱性,
故选C.
点评 本题考查溶液酸碱性判断,判断溶液酸碱性时不能根据pH判断,要根据溶液中c(H+)、c(OH-)的相对大小判断,为易错题.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
12.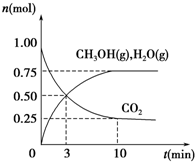 某温度下,在容积为2L的密闭容器中充入1mol CO2和3.25mol H2,在一定条件下反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化关系如图所示.下列说法错误的是( )
某温度下,在容积为2L的密闭容器中充入1mol CO2和3.25mol H2,在一定条件下反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化关系如图所示.下列说法错误的是( )
 某温度下,在容积为2L的密闭容器中充入1mol CO2和3.25mol H2,在一定条件下反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化关系如图所示.下列说法错误的是( )
某温度下,在容积为2L的密闭容器中充入1mol CO2和3.25mol H2,在一定条件下反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化关系如图所示.下列说法错误的是( )| A. | 该反应的化学方程式为CO2+3H2?CH3OH+H2O | |
| B. | 从反应开始到3 min时,氢气的平均反应速率v(H2)=0.25 mol•L-1•min-1 | |
| C. | 在原容器中再充入1 mol H2能使CO2的转化率增大 | |
| D. | 恒温下,向反应体系中加入固体催化剂,反应产生的热量增加 |
13.下列说法正确的是( )
| A. | 在101 k Pa时,1 mol C与适量O2反应生成1mol CO时,放出110.5 kJ热 量,则C的燃烧热为110.5 kJ/mol | |
| B. | 在10l k Pa时l mol H2完全燃烧生成液态水放出285.8 kJ热量,H2燃烧热为-285.8KJ/mol | |
| C. | 鉴定HCl和NaOH反应的中和热时,每次实验均应测量3个温度即盐酸起始温度、NaOH起始温度和反应后终止温度 | |
| D. | 在稀溶液中:H+(aq)+oH-(aq)=H2O(l)△H=-57.3KJ/mol,若将含0.5molH2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量等于57.3KJ |
17.NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 23gNa在空气中加热完全变成Na2O2时失去2NA个电子 | |
| B. | 标准状况下,22.4LH2含有NA个H2分子 | |
| C. | 1mol/L的硝酸钠溶液中含有的硝酸根离子数为NA | |
| D. | 0.5molKClO3中含有ClO3-的数目为NA |
7.下列叙述中,正确的是( )
| A. | 用石墨电极电解加有酚酞的饱和食盐水,由于氢氧根离子向阳极移动,所以阳极区溶液首先变为红色 | |
| B. | 在铁管上镀锌时,铁管与直流电源的正极相接 | |
| C. | 给蓄电池充电时,直流电源的正极与蓄电池的正极相接,发生氧化反应 | |
| D. | 粗铜中含有少量锌、银等金属,电解精炼该粗铜时,阳极只发生的反应是:Cu-2e-═Cu2+ |
14.下列溶液中粒子数目由多到少的顺序正确的是( )
①20mL0.01mol•L-1KCl溶液 ②30mL0.02mol•L-1CaCl2溶液
③10mL0.03mol•L-1HCl溶液 ④40mL0.01mol•L-1MgCl2溶液
⑤50mL0.05mol•L-1AgNO3溶液.
①20mL0.01mol•L-1KCl溶液 ②30mL0.02mol•L-1CaCl2溶液
③10mL0.03mol•L-1HCl溶液 ④40mL0.01mol•L-1MgCl2溶液
⑤50mL0.05mol•L-1AgNO3溶液.
| A. | ⑤>②>④>③>① | B. | ④>①>③>②>⑤ | C. | ⑤>④>②>①>③ | D. | ④>③>⑤>②>① |
11.禁止用工业酒精配置饮料,是因为工业酒精中含有某种毒性很强的醇,该醇是( )
| A. | 甲醇 | B. | 乙二醇 | C. | 丙三醇 | D. | 异戊醇 |
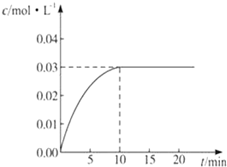 在某一容积为5L的密闭容器内,加入0.2molCO和0.2molH2O,在催化剂存在的条件下高温加热,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H>0,反应中CO2的浓度随时间变化情况如图所示:
在某一容积为5L的密闭容器内,加入0.2molCO和0.2molH2O,在催化剂存在的条件下高温加热,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H>0,反应中CO2的浓度随时间变化情况如图所示: